团队开发新的小鼠模型来揭示神秘亨廷顿氏病发病
简和特里•塞梅尔神经科学研究所的研究员和加州大学洛杉矶分校的人类行为和加州大学洛杉矶分校的大卫格芬医学院已经开发出一种新的小鼠模型的亨廷顿氏舞蹈症概括比早些时候亨廷顿氏病特征模型。提供新的线索神秘基因突变如何决定疾病发作,给研究者一个强大的新工具来测试新疗法与多个目标治疗毁灭性的神经紊乱。
亨廷顿氏舞蹈症疾病影响了超过30000人在美国根据国家神经疾病和中风研究所,引起各种症状,如人格改变,缺乏判断力,步态蹒跚和无意识的动作,说话和吞咽障碍。虽然一般在30至50岁之间开始,早期发病(20岁以下)或发病后会发生(70岁)。
亨廷顿氏病是一种家族性神经退行性疾病中一个孩子的父母在这种疾病的机率是五五开继承致病突变基因,名叫杭丁顿蛋白。的人没有亨廷顿氏舞蹈症,DNA的基因通常包含大约18重复字母C-A-G,但患有这种疾病可能40重复或更多;患者目前为止最长的延伸发现包含超过100个CAG重复。
“既然亨廷顿氏病是由单个基因突变,可以想象它应该更容易治疗干预。然而,尽管这种突变被发现大约30年前,世界各地的科学家战斗很难找到疾病修饰治疗,到目前为止,所有的努力尚未成功,尤其是在去年的承诺的停止临床试验降低突变杭丁顿蛋白的表达,这是一个挫折的高清社区,”博士说x威廉·杨的精神病学和生物行为科学教授和主席特里•塞梅尔在阿尔茨海默病的研究和治疗在加州大学洛杉矶分校的大卫格芬医学院。
这项研究由杨实验室旨在回答在亨廷顿氏舞蹈症基因奥秘。先前的研究领域集中在有毒蛋白产品由CAG重复编码,一连串的氨基酸残基(谷氨酰胺)有毒的神经元。然而,最近的人类遗传研究成千上万的HD患者透露一个意想不到的发现:CAA患者中断(CAA编码谷氨酰胺)在CAG重复后疾病的发病与患者没有这样的中断,但同样的谷氨酰胺重复。
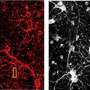
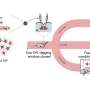
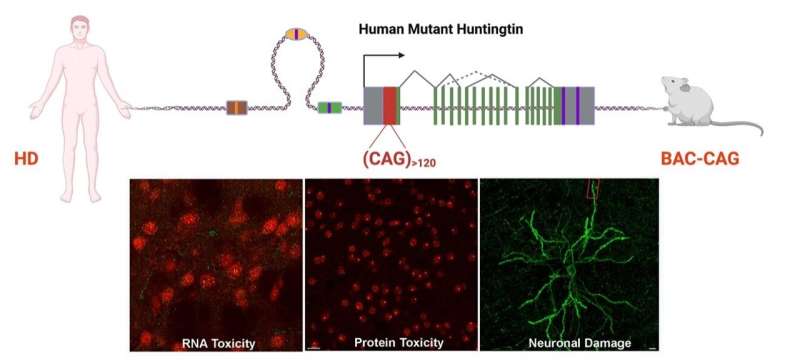
“在这项研究中,我们开发了第一个人类基因转基因小鼠模型的亨廷顿氏舞蹈症他们120 -不间断CAG重复和对比了新模型我们以前HD模型创新艺人经纪公司频繁中断。在一起,他们表明,长CAG重复是纹状体选择性毒性,控制运动和认知的大脑区域是受影响最严重的亨廷顿氏舞蹈症,”杨说。
杨,在线发表的一篇文章的资深作者2月2日,2022年,《华尔街日报》神经元补充说,其他研究结果,该研究提供了证据表明,新模型与长CAG重复可能有毒的DNA, RNA和蛋白质含量大脑区域受亨廷顿氏病发作的时候。
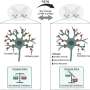
新的小鼠模型的一个子集亨廷顿氏病行为缺陷,如电动机赤字和睡眠障碍、和其他特征在很大程度上是没有在以前的小鼠模型携带人类杭丁顿蛋白的基因,如non-neuronal细胞病理变化和广泛的基因表达失调HD-vulnerable大脑区域。
“我们的新模式是独特的从治疗的角度来看,整个人类杭丁顿蛋白的基因,包括一些DNA变异存在于病人,它有一个长和纯CAG重复,”第一作者Xiaofeng顾博士说,中心的项目科学家在塞梅尔神经行为遗传学研究所曾主要负责工程和描述鼠标模型。
加州大学洛杉矶分校的新模型在塞梅尔研究所开发的可用于测试候选人疗法降低人类杭丁顿蛋白和那些针对毒性源于杭丁顿蛋白的纯CAG重复说,它还可以用来测试组合疗法针对这两种类型的目标。目前,新模型已经使用两个制药公司和一些学术实验室测试他们的治疗干预措施。
更多信息:x威廉·杨不间断CAG-Repeat驱动器Striatum-Selective Transcriptionopathy人类杭丁顿蛋白和核病机BAC老鼠,神经元(2022)。DOI: 10.1016 / j.neuron.2022.01.006。www.cell.com/neuron/fulltext/s0896 - 6273 (22) 00006 - x