治疗耐药癌症的有希望的方法
如3月7日的自然通讯在美国,研究人员使用两种药物组合来实现化疗的目标:通过被称为凋亡的生物过程使癌细胞自我毁灭,这种生物过程通常被称为程序性细胞死亡。这种治疗方法对尽管暴露于不同类型的化疗仍抵抗凋亡的人类癌细胞株有效,也对移植到小鼠(即异种移植小鼠模型)中的抗凋亡的人类肿瘤有效。
Evripidis Gavathiotis博士是爱因斯坦的生物化学和医学教授,也是国家癌症研究所指定的阿尔伯特·爱因斯坦癌症中心癌症治疗项目的联合负责人,也是这篇论文的通讯作者,他说:“针对癌症特定遗传弱点的靶向疗法近年来大大改善了治疗,但并不是每个人都受益。”“我们需要新的、广泛有效的治疗方法,能够治疗多种癌症,同时比现有的治疗方法产生更少的副作用,我们希望我们的新治疗策略将被证明是一个可行的选择。”
清除无用细胞
人体依靠细胞凋亡来清除不需要的细胞——例如,在胚胎发育过程中被修剪掉的多余细胞,以及需要移除的受损细胞,这样它们就不能存活下来发展成癌细胞。化疗和放疗都依赖于对癌细胞的严重破坏,使它们发生凋亡——不幸的是,这并不总是发生。
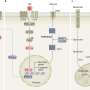
人体内的每一个细胞都包含着自身毁灭的种子:大约二十多个凋亡蛋白参与着生死平衡的行动。一些蛋白刺激细胞凋亡(促凋亡蛋白),而另一些蛋白阻断细胞凋亡(抗凋亡蛋白)。例如,DNA损伤,使天平向有利于细胞死亡-导致细胞表达和激活促凋亡蛋白,最终通过在线粒体上戳洞杀死细胞。加瓦约蒂斯博士和他的同事发现的这种新药物组合,通过促进一种促凋亡蛋白的活性形式,特别是BAX,杀死了抗凋亡的癌细胞。BAX被称为“刽子手蛋白”。
增强“刽子手蛋白质”
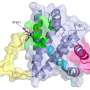
2012年,加瓦约蒂斯博士发现了第一个能够直接激活BAX的人造小分子。在他们的新研究中,他和他的团队评估了btsa1.2——他们的第三代BAX激活剂——是否能对46种不同的人类血液和实体肿瘤细胞系有效,包括非小细胞肺癌、乳腺癌、结肠直肠癌、胰腺癌、黑色素瘤、白血病和淋巴瘤细胞系。这些细胞系大多对目前开发的所有促凋亡药物都产生了耐药性。
BTSA1.2对几种实体肿瘤细胞系的作用不明显。问题是:即使BTSA1.2增加了实体肿瘤细胞中活性促凋亡BAX的水平,一种名为BCL-XL的抗凋亡蛋白却在中和BAX。随后,研究人员设计了一种杀死抗凋亡癌细胞的新策略:将促进bax的BTSA1.2与抑制BCL-XL的促凋亡癌症药物纳维托克拉(Navitoclax)结合。
BTSA1.2和Navitoclax的结合被证明是游戏规则的改变者。当Gavathiotis博士和他的同事们(由共同第一作者Andrea Lopez博士领导)在46个细胞系上测试了这种药物组合时,它形成了一种双管齐下的效果,BTSA1.2将癌细胞中的活性BAX提升到有毒水平,而Navitoclax则通过阻止BCL-XL中和BAX来充当BAX的保镖。
限制副作用
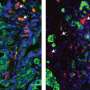
然后测试这两种口服药物对抗凋亡的肿瘤异种移植瘤的影响——在本例中,小鼠被植入结肠直肠肿瘤细胞癌症该细胞系对BTSA1.2和纳维托克拉作为单独药物产生了耐药性,但在它们联合使用时屈服。体内实验产生了类似的结果:在异种移植建立后,小鼠分别接受BTSA1.2、纳维托克拉或两种药物联合治疗。单独来看,每种药物在抑制肿瘤生长方面的效果有限,而联合使用则显著抑制肿瘤生长,这表明两种药物协同作用,可以击败抗凋亡肿瘤。
“同样重要的是,接受两种药物联合治疗的小鼠的耐受性非常好,”Gavathiotis博士指出。此外,对接受治疗的小鼠的分析表明,健康细胞不受两种药物组合的影响,这可能使其比标准化疗更安全,标准化疗对所有细胞分裂都是有毒的细胞包括癌症和正常。”