FDA对实验性渐冻症药物的疗效表示怀疑

联邦卫生监管机构周一对一种受到密切关注的实验性药物发布了负面评论,此前患者权益倡导者进行了数月的游说,敦促批准这种药物。
Amylyx制药公司的这种药物已经成为致命神经退行性疾病渐冻人症(ALS)患者、他们的家人和国会议员的集结原因,他们加入了推动美国食品和药物管理局(fda)为这种药物开绿灯的行列。
但监管机构在一份审查报告中表示,该公司的小型研究“缺乏说服力”,原因是数据缺失、患者登记错误和其他问题。周三,FDA顾问小组将就是否批准该药物进行不具约束力的投票。
此次会议受到密切关注,被视为FDA在数据不完善的情况下处理实验性药物的方法及其承受外部压力的能力的一个指标。
FDA对该药物的负面立场在周三的公开会议上造成了紧张的局面,数十名渐冻人症患者和倡导者将在会上发言。该机构将考虑其顾问小组的意见,然后对该药物做出最终决定,预计将于6月做出最终决定。
ALS(肌萎缩性侧索硬化症)会破坏行走、说话、吞咽以及最终呼吸所需的神经细胞。目前尚无治愈方法,大多数人在三到五年内死亡。
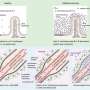
Amylyx的药物是两种较老药物的组合:一种是治疗肝病的处方药,另一种是与中药有关的膳食补充剂。Amylyx已经将这种混合物制成粉末申请了专利,并表示这种化学物质有助于防止细胞过早死亡。
但审稿人发现,在一项涉及137名患者的中期研究中,该药物对减缓疾病进展的作用“不大”,审稿人表示,该研究存在实施和分析问题。通常情况下,FDA的批准需要两项大型研究或一项对生存有“非常有说服力”影响的研究。
根据FDA的文件,监管机构“强烈建议”Amylyx在应用前完成一项大型后期试验,以确定药物的有效性。这项研究将于2024年完成。
去年夏天,经过与监管机构的进一步讨论,Amylyx决定根据最初的研究和随后收集的生存数据,将其药物提交审批。该公司表示,数据显示,服用该药的患者比服用假药的患者寿命长约6个月。
但FDA表示,由于跟踪研究参与者数年存在问题,因此结果不可靠。
周三的会议标志着FDA自去年6月无视其建议并批准Biogen的阿尔茨海默病药物Aduhelm以来首次召集该顾问团。三名小组成员因这一有争议的决定辞职,国会调查人员对FDA对该药物的审查进行了调查。就像目前的情况一样,FDA面临着来自患者群体的巨大压力,要求批准。
目前,只有两种fda批准的治疗肌萎缩性侧索硬化症的药物,其中较有效的一种可以延长几个月的寿命。
资助Amylyx研究的渐冻症协会(ALS Association)表示,FDA的审查没有考虑到“渐冻症的速度和严重程度,以及可用的治疗方案很少。”
约翰霍普金斯大学的杰弗里·罗斯坦博士帮助招募了Amylyx研究的患者,他说:“这是一种致命的疾病,所以任何显示出这种益处的药物——即使这种益处不大——对患有这种疾病的患者来说都是极好的,他们只有一条路可走:死亡。”
在FDA公布审查报告后,这家总部位于马萨诸塞州剑桥的制药商的股价周一下跌了35%以上。
___
这个故事已被更正,注意到这种药物是粉末,而不是药丸。
©2022美联社。版权所有。未经允许,本材料不得出版、广播、重写或再分发。