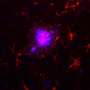
新战略可以减少脑损伤在阿尔茨海默氏症和相关疾病的老鼠
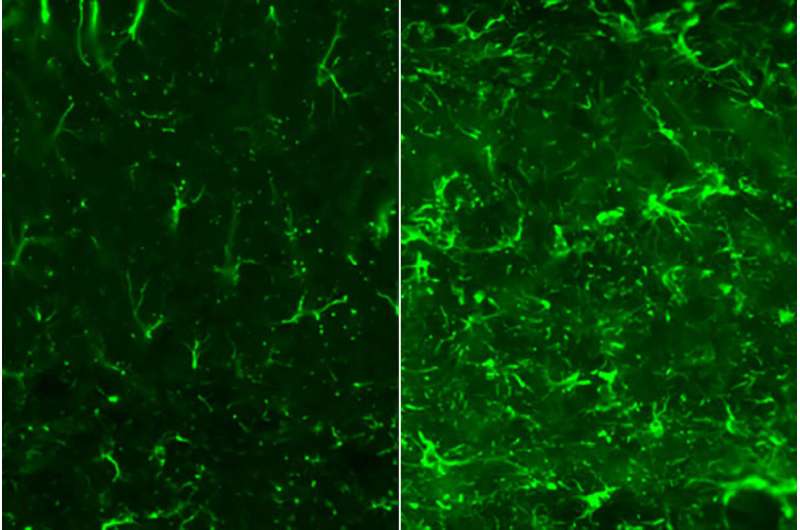
阿尔茨海默病是最常见的和最著名的tauopathies,一组大脑神经退行性疾病引起的有毒蛋白质τ的缠结。一项由圣路易斯华盛顿大学医学院的研究人员已经表明,针对astrocytes-an炎性细胞在brain-reduces tau-related脑损伤和炎症在老鼠身上。
结果,网上《科学—转化医学》突出星形胶质细胞的关键作用在tauopathies驾驶脑损伤,并打开更好的治疗的新途径的毁灭性的和难以治疗条件。
“大脑炎症正在成为一个贡献者阿尔茨海默病的发展,这是由非炎症神经细胞在大脑中,包括星形胶质细胞,”吉尔伯特Gallardo资深作者说,博士,神经病学助理教授。“我们的研究突显出,星形胶质细胞发炎导致tau-associated病态,表明压制他们的反应可能是有益的在减少脑部炎症和延缓老年痴呆。”
τ,通常发现在大脑中的神经元,有助于形成内部脚手架,使神经元的形状。当τ变得复杂,它会导致大脑炎症、组织损伤和认知能力下降。τ形成缠结的人携带τ基因的突变或有经验的攻击等大脑重复脑震荡或暴露于神经毒性的化学物质。在阿尔茨海默氏症,τ缠结形成相对较晚在疾病过程中,显然由早些时候引发疾病的大脑变化如蛋白质β淀粉样蛋白斑块的形成。
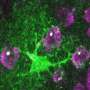
在许多神经退行性条件,所谓无功astrocytes-astrocytes激活,这样他们造成伤害,而不是保护神经元损伤的大脑组织丰富的网站。在以前的工作肌萎缩性脊髓侧索硬化症(肌萎缩性侧索硬化症),神经退行性疾病,但不是tauopathy,盖拉多和他的同事发现了一个星形胶质细胞蛋白质,鼓励细胞毒性特征和加重脑部炎症。盖拉多怀疑蛋白质,名叫alpha2-Na + / K +三磷酸腺苷酶(alpha2-NKA),也可能推动星形胶质细胞的毒性在阿尔茨海默病和其他tauopathies。
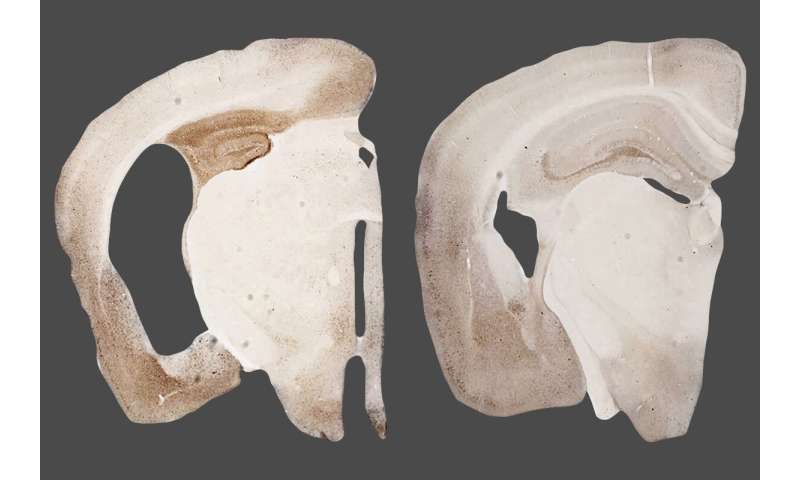
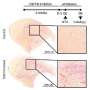
盖拉多,第一作者卡洛琳曼,然后盖拉多的实验室的技术人员,和合作者Celeste Karch,博士,精神病学的副教授,获得数据alpha2-NKA编码基因的表达水平。他们研究了大脑样本80人死于阿尔茨海默氏症;82人死于tauopathy调用进行性核上的麻痹(PSP);和76年去世的原因与神经退化无关。研究人员发现alpha2-NKA高度表达的人死于阿尔茨海默氏症或PSP相比之下,那些死于其他原因,表明蛋白质可能是一个因素在两种情况下脑损伤。
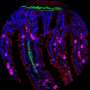
进一步调查alpha2-NKA所扮演的角色,研究人员把小鼠转基因开始发展τ缠结约6个月的年龄。½9个月大的时候,这种动物的大脑受损、萎缩和发炎,他们已经失去了正确执行日常任务的啮齿动物生活的能力如筑巢。研究人员发现,与tauopathies像人一样,转基因小鼠在他们的大脑也alpha2-NKA水平升高的。水平上升为老鼠长大和炎症脑损伤恶化。
地高辛,用于治疗的药物心脏病,干扰alpha2-NKA的活动。研究人员测试了地高辛治疗小鼠是否能减少τ缠结,大脑萎缩和炎症和行为变化。药物工作,此外,它是否给老鼠的复合工作在6个月大的时候,当动物们刚刚开始开发τ缠结,或在8个月,缠结和破坏已经建立了。
“这里的关键信息是,抑制发炎星形国家停止疾病进展,”曼恩说。“这是很重要的,因为实验治疗阿尔茨海默氏症和相关tauopathies很大程度上集中清算病理蛋白质,与神经功能障碍和死亡。但我们的研究证据表明,针对发炎星形胶质细胞和大脑炎症可能是成功治疗的关键条件。”
地高辛时已通过美国食品和药物管理局对某些心脏病,其影响大脑前必须进行更彻底地评估作为一个潜在的治疗阿尔茨海默氏症和相关tauopathies,盖拉多说。