病理图像质量自动评估
用于癌症诊断和治疗的组织样本分析仍主要在光学显微镜下完成。但研究人员现在正在开发技术,通过对组织活检图像的数字化和计算机辅助分析来加快并最终提高诊断的准确性。这些新技术在很大程度上依赖于人工智能(AI)工具,这需要在与临床结果数据相关联的数字化整张幻灯片图像(WSIs)的大型数据集上开发和“训练”人工智能算法。但是,从多个诊断实验室整理的图像在质量上可能有很大差异,这反过来又会影响人工智能算法的训练和后续性能。
新出版的刊物科学报告由路德维希·牛津大学的延斯·里切尔和他在牛津大学的同事玛丽亚姆·哈格海特领导的研究小组描述了一种人工智能一个名为PathProfiler的工具,可以自动化大型回顾性病理图像数据集的质量控制,以提高其在下游研究中的可用性。
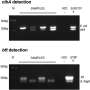
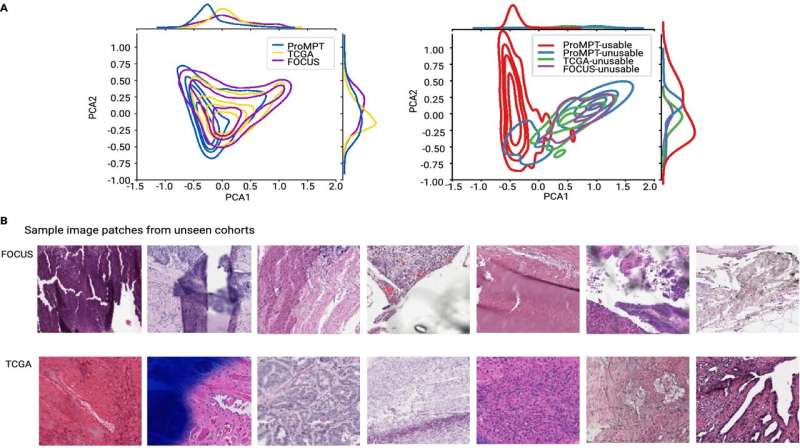
Rittscher和他牛津大学的同事利用前列腺癌进展和治疗机制(ProMPT)前列腺的回顾性病理图像开发了PathProfiler癌症队列。他们的AI工具可以自动评估病理图像的质量,并识别一系列潜在的图像伪影。它还为每个WSI分配了一个可用性评分,这将有助于指导图像是否可以包含在AI训练数据集中。AI算法生成的分数与三位病理专家分配的分数高度相关(0.89)。
为了进一步测试PathProfiler,研究小组评估了癌症基因组图谱前列腺癌和FOCUS结直肠癌队列。除了在WSIs中提供质量评分和识别影响质量的工件外,PathProfiler还能够预测哪些图像可以通过重新扫描或重新染色来改进。这一预测与高度策划的回顾性队列样本的可用性特别相关,例如前列腺癌研究中使用的样本。
的PathProfiler软件可供公众使用,以便其他小组可以使用它进行自己的研究,并为其进一步发展做出贡献。该团队现在计划使用其他组织类型和队列进一步优化模型,并在临床病理数字管道中评估该工具的性能和效用。
更多信息:Maryam Haghighat等人,人工智能对大型数字化组织学队列的自动化质量评估,科学报告(2022)。DOI: 10.1038 / s41598 - 022 - 08351 - 5