免疫细胞中的关键信号通路可能是阿尔茨海默病的新靶点
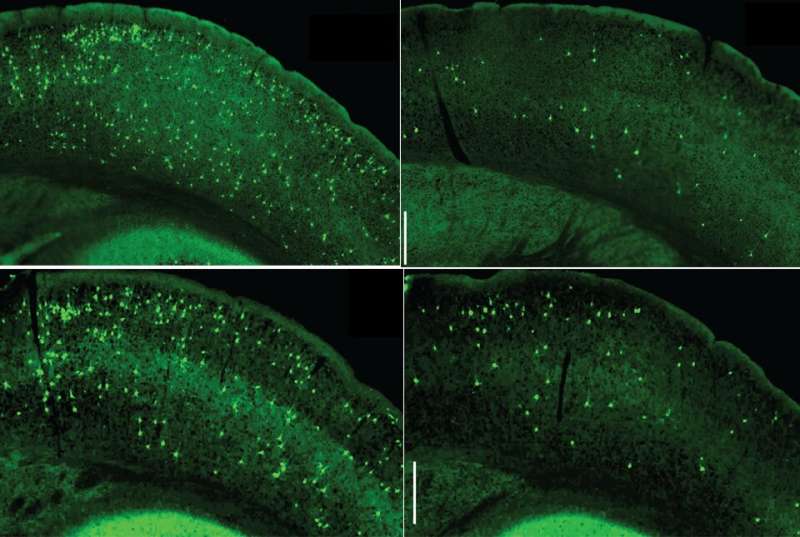
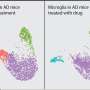
威尔康奈尔医学院的一项研究表明,抑制脑内免疫细胞的一种重要信号通路可能缓解大脑炎症,从而减缓阿尔茨海默症和其他一些神经退行性疾病的发病过程。这一发现指出了针对神经退行性疾病的新治疗策略的可能性。神经退行性疾病在老年人中相对常见,迄今为止还没有有效的、改善疾病的治疗方法。
长期以来,人们一直认为大脑炎症是神经退行性疾病的共同特征,尤其是通过激活大脑中称为小胶质细胞的免疫细胞引起的炎症。一种叫做tau的神经蛋白的异常线状聚集物(“缠结”)的扩散是这些疾病的另一个常见特征。
该研究发表在4月12日的自然通讯研究人员发现,tau蛋白缠结通过一种称为NF-κB通路的多功能信号通路,有助于触发小胶质细胞的炎症激活。在以陶蛋白为基础的阿尔茨海默氏症小鼠模型中,抑制小胶质细胞NF-κB信号在很大程度上使免疫细胞脱离炎症状态,逆转了动物的学习和记忆问题。
“我们的研究结果表明,抑制过度活跃的NF-κB可能是阿尔茨海默症和其他tau介导的神经退行性疾病的一个很好的治疗策略,”高级作者李甘博士说,他是海伦和罗伯特阿佩尔阿尔茨海默症研究所的主任,以及威尔康奈尔医学院费尔家族脑与精神研究所神经退行性疾病的Burton P.和Judith B. Resnick特约教授。
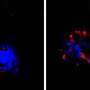
Tau缠结存在于受影响的神经元内部大脑区域阿尔茨海默病帕金森病皮克病进行性核上的麻痹额颞叶痴呆等神经退行性疾病.实验表明,当把这些缠结注射到动物大脑中时,可以为新的缠结的形成埋下种子,形成一个连锁反应,使缠结扩散到大脑的其他区域。对阿尔茨海默氏症和其他“牛皮病”的尸检研究表明,这种缠结的扩散往往与疾病的进展密切相关。
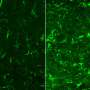
神经缠结在伤害脑细胞方面的确切作用从未被完全了解。然而,先前的研究表明,tau蛋白缠结可以与小胶质细胞相互作用,以一种方式驱动小胶质细胞进入炎症,疾病相关的状态。在这种发炎的状态下,通常试图消耗tau蛋白缠结的小胶质细胞变得相对低效。大部分tau蛋白最终没有被消化,而是从小胶质细胞中释放出来,这种形式往往会产生新的缠结。
在这项新研究中,甘博士和她的团队从细胞培养和小鼠实验中发现,tau蛋白缠结主要通过激活小胶质细胞内的NF-κB信号通路,将小胶质细胞推入这种与疾病相关的炎症状态。在一种主要由tau蛋白驱动的阿尔茨海默氏症小鼠模型中,他们表明,保持小胶质细胞中NF-κB通路的过度活性可以增强缠结的播撒和扩散,从而进一步促进NF-κB激活。相反,关闭NF-κB阻断了这种恶性循环,并显著减少了缠结的扩散。
在另一个tau蛋白小鼠模型中,衰老神经元中形成tau蛋白缠结,研究人员表明,小胶质细胞NF-κB失活使小胶质细胞几乎完全脱离炎症和疾病相关状态,恢复了更正常的细胞外观和基因活性模式。这种转变,抑制了小神经胶质细胞令人惊讶的是,从排泄有毒的tau蛋白种子,阻止了在这个模型中正常发展的小鼠的关键认知/记忆缺陷。
“总的来说,我们的实验表明,tau蛋白对认知的毒性作用需要小胶质细胞NF-κB信号,”共同资深作者罗文杰博士说,他是阿佩尔阿尔茨海默病研究所和威尔康奈尔大学费尔家族脑与心智研究所神经科学研究的副教授。
在过去的20年里,许多实验性的阿尔茨海默症治疗都旨在通过靶向治疗来减缓或停止疾病进程淀粉样斑块,最近τ缠结.到目前为止,所有这些努力都在大规模临床试验中失败了。甘博士说,新的发现表明,未来驯服过度活跃的小胶质细胞NF-κB信号的药物可能效果更好。
她的实验室现在正在进行进一步的研究,以更精确地了解小胶质细胞NF-κB信号是如何影响至少数百种其他小胶质基因的活动,从而损害神经元并导致认知和记忆缺陷的。研究人员将研究如何在不影响大脑正常功能的情况下抑制过度活跃的NF-κB信号的特定方面免疫细胞.
进一步探索