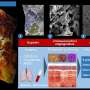
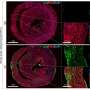
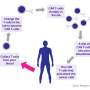
具有特定基因调控模式的白血病患者对CAR - T治疗的反应可能较低
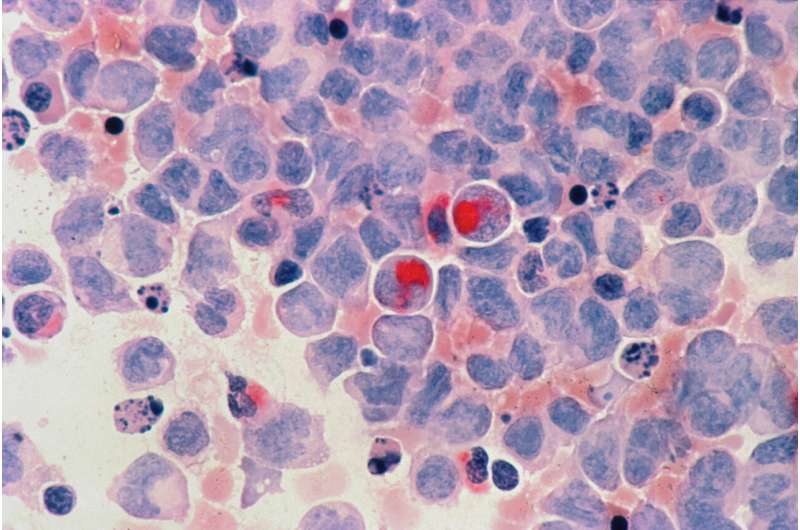
根据在4月8日至13日举行的AACR 2022年会上公布的结果,来自对cd19靶向CAR - T疗法无反应的患者的急性淋巴细胞白血病(ALL)细胞具有基因调控特征,可能会促进治疗耐药。
“我们在治疗前发现了一种无反应的信号,并且可以检测到,”国家癌症研究所遗传学分支的nih -剑桥学者Katherine Masih说,她介绍了这项研究。
她补充说:“数据支持这些白血病具有相对的可塑性,并表现出多谱系的潜力,类似于干细胞,我们怀疑这使它们能够更快地适应CD19 CAR - T细胞的进化压力。”
CAR - t细胞疗法是一种免疫疗法免疫细胞一种叫做T细胞的细胞从病人身上提取,重新编程,以达到目标癌症细胞然后注入到病人体内以对抗癌症。CAR - t细胞的一个常见靶标是受体CD19;然而,癌细胞可以突变CD19或抑制其表达来产生CAR - T抗性。虽然CD19的表达目前是潜在CAR - T反应的少数生物标志物之一,但并不是所有产生耐药的患者都失去了CD19的表达。
“我们的研究是少数着眼于CAR - T治疗原发性无反应的cd19独立来源的研究之一,”该研究的资深作者、国家癌症研究所遗传学部副主任Javed Khan医学博士说,他解释说,一些细胞在本质上容易产生治疗耐药性。“主要目的是确定已经存在的、白血病固有的耐药性机制。”
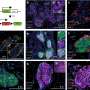
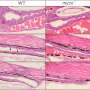
研究人员从plato -02临床试验中获得了预处理骨髓样本,该试验在西雅图儿童医院与Rebecca Gardner医学博士和Rimas Orentas博士合作进行。样本来自7名在cd19靶向CAR - T治疗后完全缓解的患者,以及7名在治疗后63天内循环白血病细胞持续存在的无反应患者。他们使用几种细胞谱分析方法对白血病细胞进行了全面的特征描述,例如whole-exome测序、大块细胞群的RNA测序、单细胞RNA测序、基于阵列的甲基化分析和ATAC-seq(一种定位经常表明增加的可及染色质区域的检测方法)基因表达.
研究人员发现了区分CAR - t抵抗性白血病细胞和CAR - t反应性白血病细胞的基因调节机制的三个显著特征。一种是DNA甲基化模式——一种减少基因表达的调节标记——与干细胞样表型相关。
“我们观察到在胚胎细胞中已知的被抑制的基因周围的高甲基化癌症干细胞,”·马西说。
Masih和他的同事在检查白血病细胞的DNA可及性谱时观察到类似的结果。CAR - t细胞耐药性白血病的开放染色质区域与干细胞增殖有关,并与造血祖细胞中发现的模式相似,包括造血干细胞和髓样细胞的祖,髓样细胞是与CAR - t细胞相关的不同类型的血细胞急性髓系白血病(AML)。
Khan说,从淋巴系到髓系的转变已经被观察到是CD19-CAR - T治疗耐药的机制。“有趣的是,我们看到表达淋巴和髓系标记的细胞亚群,这表明一些无反应性白血病的表观基因组可能包含ALL和AML表观基因组的杂交细胞群,”Khan说。“我们的数据表明,这些白血病的特征是淋巴和骨髓特异性可及区域,可能比反应性白血病的分化程度低。”
研究人员还发现,在对CAR - T疗法没有反应的细胞中,参与抗原呈递和处理的基因表达减少,而抗原呈递和处理是建立免疫反应的关键途径。抗原呈递的减少可能表明,即使白血病细胞继续表达CD19,它们也可能无法有效处理额外的免疫靶点。
“我们下一步将在老鼠模型中重现这种临床现象,使用不同的亚群体白血病细胞,然后检查我们是否可以通过组合或替代疗法克服这种初级耐药性,”Masih说。
Khan补充说:“这项研究让我们不仅能够识别潜在的临床生物标志物,还可以测试使用这些分析方法影响患者护理的后勤可行性。”“我们希望有一天,对这种表型的筛查可以让临床医生识别出那些在治疗前不太可能有反应的白血病患者,并提供替代疗法来改善这些患者的预后。”
本研究的局限性包括样本量小。