2022年4月12日,功能
艾滋病毒测序前病毒从人们使用droplet-microfluidics抗逆转录病毒治疗
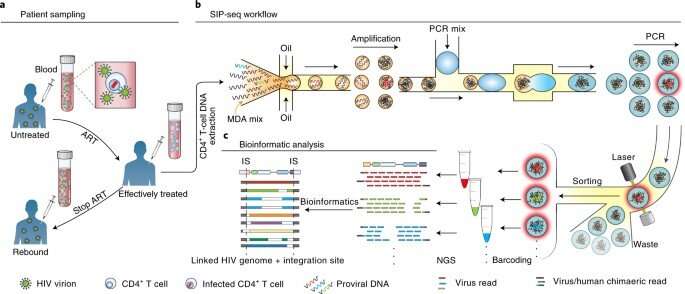
人类免疫学病毒(HIV)的感染发生通过整合其基因组到感染细胞进入一个可逆的非活动状态延迟,避开抗逆转录病毒疗法。序列的能力这样的前病毒和相邻的主机连接在单个细胞可以强调他们在感染细胞的作用机制和持久性。然而,这个实验是很难执行由于高1.5亿倍的背景人类DNA。现在发表在一份新报告自然生物医学工程陈,太阳和一个研究小组在生物工程和病毒持久性和动力学研究的加州大学,旧金山,NIH和陈扎克伯格Biohub,在美国,showed how full-length proviruses are connected to the HIV-host DNA junctions via high-throughput microfluidic assays, for droplet-based whole genome amplification of HIV DNA in its native context. The team conducted a polymerase chain reaction (PCR) to tag droplets containing proviruses to sequence and assay infected cells from people with HIV, receiving suppressing antiretroviral therapy at the time to detect and sequence paired proviral genomes and integration sites. The work sought to improve genetic analysis of persistent HIV-infected cell reservoirs.
艾滋病毒治疗的现状和发展的治疗策略
而全世界大约有3700万人感染人类免疫缺陷病毒(艾滋病毒),治愈仍然未知。病毒的感染机制规定了中央的障碍,还拥有治愈疾病的关键,作为其基因组艾滋病毒整合到感染细胞的基因组。尽管抗逆转录病毒疗法(ART)可以抑制病毒复制到检测不到的水平,防止病情发展获得性免疫缺陷综合症(艾滋病),它缺少活动细胞水库。结果,治疗必须继续无限期地防止病毒反弹和疾病进展。很难解决艾滋病污名,由于终身艺术管理的成本,用有毒的潜力。因此重要的是要消除或抑制艾滋病毒感染细胞水库获得功能性治愈。检查细胞水库的持久性,科学家必须进行配对分析集成网站和完整的前病毒序列。通过建立可靠、节省成本的方法,分离和序列罕见的病毒?,研究人员可以全面描述HIV水库。太阳等开发这种方法描述前病毒和细胞基因组上下文在艾滋病毒水库使用同步集成网站和前病毒测序(SIP-Seq)。
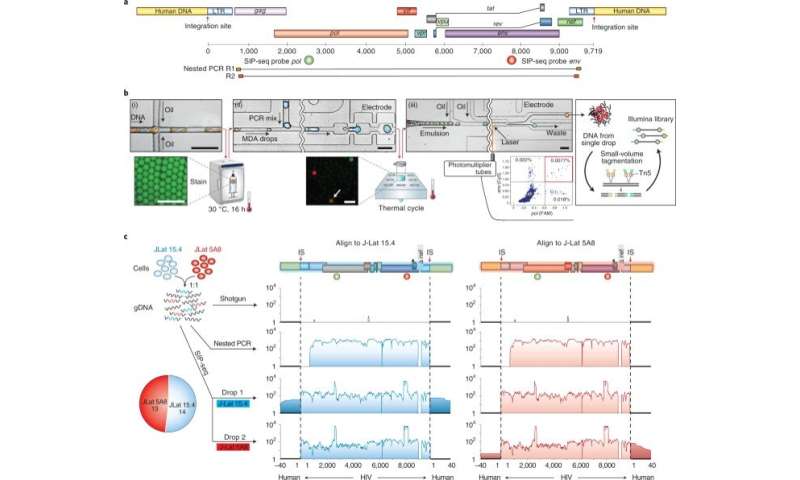
利用全基因组测序放大、太阳等扩大艾滋病毒基因组在本土环境在微流控液滴,然后为测序标记包含原病毒的飞沫。由此产生的方法提供了一个完整的病毒基因组与宿主细胞连接通过一个连续的组装。该方法的速度和效率允许单前病毒基因组的复苏1.5亿倍高背景的DNA。该团队使用SIP-Seq(同时集成网站和前病毒测序)配置文件前病毒人群在各种艺术相关个人理解潜在的HIV水库。当团队关注艾滋病,这种方法适用于不同的病毒入侵宿主的基因组,提供一个通用平台,描述各种感染的基因。
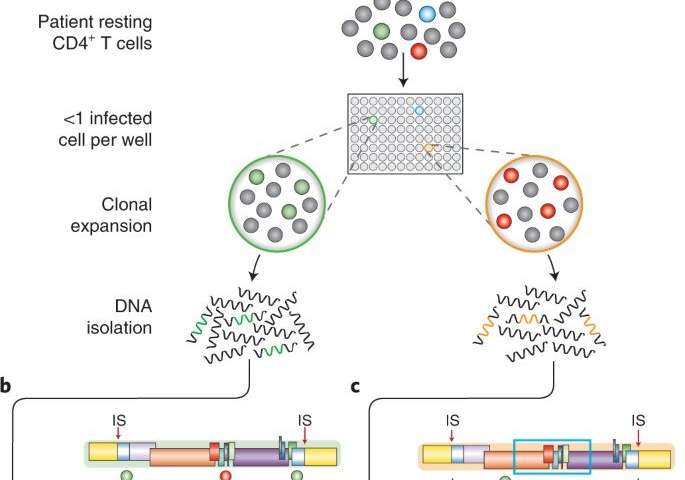
实验
太阳等旨在恢复所有含有艾滋病毒的基因组DNA片段从数以百万计的人口CD4+T细胞单独序列的分子,他们立即相邻路口。团队从细胞中提取DNA片段大封装在微分离集成艾滋病毒基因组。使用多路复用位移放大(MDA),他们流感放大每个基因片段测序获得足够的单前病毒。他们随后通过孤立个体携带HIV病毒的飞沫前病毒,其中每个液滴页码和测序。病毒学家然后映射读数从每个液滴艾滋病毒基因组参考识别集成网站促进明确的信息在病毒基因组的复杂性,及其集成sites-crucial评估细胞的水库。
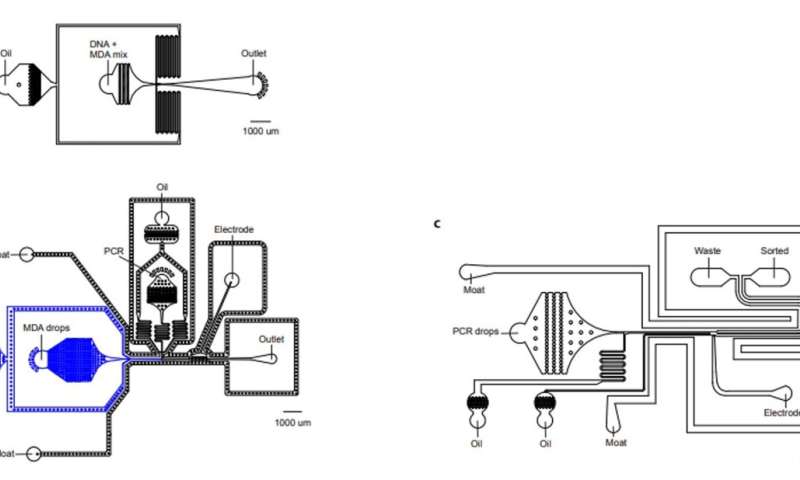
检测前病毒SIP-Seq和调节微流体
增加全身前病毒的特异性和防止随机DNA乳沟,太阳等采用双重具体多路复用Taqman PCR目标地区,艾滋病毒基因组。在实验中,他们产生了特定的DNA序列和体积确认艾滋病前病毒复苏。的微流体SIP-Seq设置包含三个设备,包括一个液滴encapsulator,合并和分选机。科学家把人类基因组DNA片段与多个位移放大(MDA)试剂来封装100亿DNA片段,逼近75年kbp的长度,2000万年独立的水滴,在15分钟。每个液滴含有500不同的片段和太阳等孵化在30摄氏度,为非特异性扩增,合并前Taqman PCR试剂。重复这个步骤之后发现艾滋病毒基因组,团队准备测序的管子。
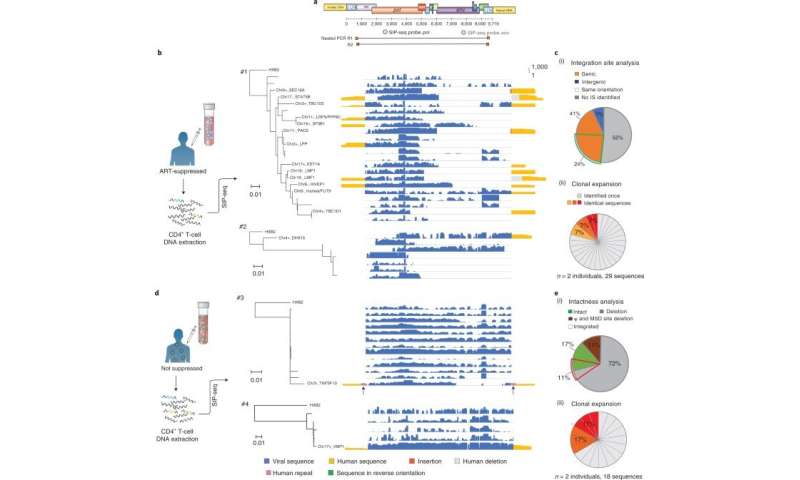
分析艾滋病前病毒及其基因组景观ART-treated人
阳光下验证等SIP-Seq艾滋病细胞系和分析艾滋病毒抗逆转录病毒治疗的人。在实验中,他们准备细胞通过电镀,CD4休息+刺激T细胞从一个ART-treated人,其次是通过三个方法和体外培养增殖;散弹枪,嵌套PCR和SIP-Seq Taqman调查。SIP-Seq和嵌套PCR取得了优秀的结果,团队专门选择了SIP-Seq感染细胞体内的全部遗传多样性特征。他们按照这个工作描述艾滋病前病毒的基因组景观,它们直接分离CD4 + T细胞被感染的人。结果显示三个克隆支持克隆起源相对于血统先前的研究相同的个体。
前景
研究表明方法如何使陈太阳和他的同事们研究艾滋病毒前病毒比与现有的PCR方法更有效。结果提供了一个综合分析体内的艾滋病病毒的遗传景观特征的储层中突显其作用HIV持久性。现有方法挑战由于稀有和缺乏独特的表面标记来识别潜伏性感染细胞。使用描述SIP-Seq(同步集成网站和前病毒测序)方法,太阳等提供了一种快速、成本效益和可伸缩的过程,它们应用于人们接受抗逆转录病毒疗法(艺术),强调潜在的水库的存在无性生殖细胞扩张。战略在艾滋病毒感染,适用于其它病毒性疾病与集成在他们的生命周期。
进一步探索
凯瑟琳·m·布鲁纳等储层的定量方法来衡量潜在的hiv - 1病毒,自然(2019)。DOI: 10.1038 / s41586 - 019 - 0898 - 8
©2022科学欧宝app网彩X网络