利用碱基编辑技术开发复发或难治性T-ALL的异基因嵌合抗原受体t细胞
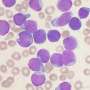
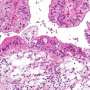
费城儿童医院(CHOP)的一组研究人员与Beam Therapeutics合作,使用碱基编辑测试并开发了一种“现成的”嵌合抗原受体t细胞(CART),旨在对CART进行精确编辑,降低其他编辑方法可能伴随的不必要和不可预见的结果的风险。CART被称为7CAR8,最近在杂志上的一篇论文中进行了描述血在多种临床前模型中,对t细胞急性淋巴母细胞白血病(T-ALL)具有高度活性。在复发或难治性疾病的背景下,T-ALL通常对化疗无反应,治愈的机会很低。如果获得批准,7CAR8有望成为这些患者有效的救命疗法。
CAR - t细胞疗法已经彻底改变了复发性或难治性血癌的治疗,有几种产品获得了美国食品和药物管理局(FDA)的批准。然而,这些产品涉及从癌症患者身上获取和修饰T细胞,这带来了许多挑战。由健康捐赠者创建的CART将绕过许多这些问题,并有可能提供按需的“现成”产品。这样的产品需要修改以防止移植物抗宿主病(GVHD)和患者免疫细胞的CART排斥反应。
为了解决这些障碍,研究人员使用基因组编辑修改了异基因CART产品,但其中许多工具(如crispr - cas9)依赖于DNA双链断裂(dsb),这可能导致意想不到的结果,并可能导致不可预见的后果。这些不良结果具有重大的临床意义,并可能危及以这种方式生产的“现成”CART的批准或应用。
基编辑是一个新兴技术能够在特定的点上进行单碱基对的变化,精度高,效率高。碱基编辑器是为消音而设计的基因表达而不产生dsb,与CRISPR-Cas9等技术相比,可能会减少不希望的编辑结果。
为了确定碱基编辑产生CART在临床上是否可行,CHOP的研究人员,由癌症中心的主治医生Caroline Diorio博士领导,并与Beam Therapeutics合作,测试了一种“现成的”CART用于复发或难治性T-ALL,靶向表面受体CD7,它在绝大多数T-ALL细胞中高度表达。鉴于CD7也在健康细胞表面表达,研究人员使用胞嘧啶碱基编辑进行了四次碱基编辑,以创建7CAR8,这被认为是第一个同时进行四次基因编辑的CAR - T产品,正朝着临床开发的方向发展。
在体内和体外都有多种临床前研究,研究人员观察到7CAR8不影响t细胞增殖或导致基因组重排产物。他们还观察到7CAR8在体外和体内的细胞系模型和多个患者来源的T-ALL异种移植(PDX)模型中具有高度活性。该研究的共同作者、主治医生Sarah K. Tasian医学博士目前正在另一种儿童癌症——急性髓系白血病(AML)的临床前模型中测试这种疗法。
实验室的研究表明7CAR8在体内高度活跃临床前模型如果获得批准,可能会成为儿童和成人复发或难治性T-ALL的治疗方法。它也有可能用于其他CD7+恶性肿瘤的治疗,如t细胞淋巴母细胞淋巴瘤和亚群急性髓系白血病高级研究作者David T. Teachey医学博士说,他是CHOP儿童癌症研究中心的主治医生和临床研究主任。“基于这些结果,我们计划将7CAR8转化为复发或难治性T-ALL儿童和成人的临床治疗。这种高度适应性的编辑方法也有可能用于为其他免疫治疗靶点创建‘现成的’car。”
进一步探索