一种新方法therapy-resistant肿瘤目标特定的细胞死亡通路
在一篇文章中出现自然今天,一个国际科学家小组报告杀死不易治愈癌症的新方法。这些抵制目前肿瘤免疫疗法,包括那些使用诺贝尔奖获得者checkpoint-blocking抗体。
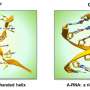
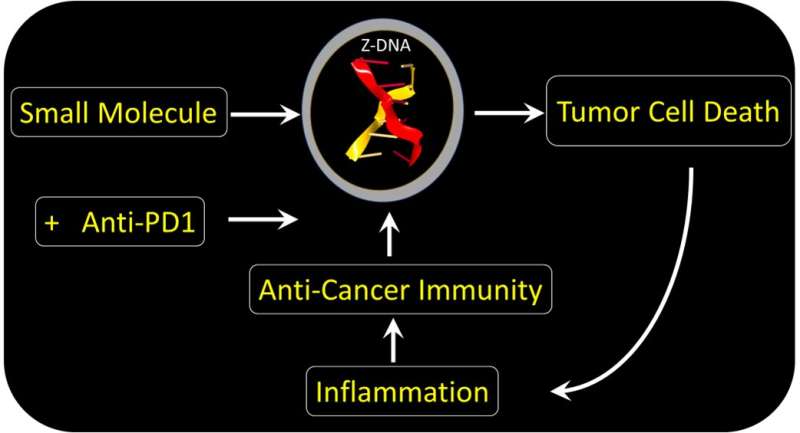
该方法利用Z-DNA。而不是像B-DNA扭向右,Z-DNA左旋扭。一个角色Z-DNA调节免疫反应病毒。响应AADR1 ZBP1,涉及两个专门识别Z-DNA蛋白质。他们这样做的时候通过一个Zα域与高亲和力结合Z-DNA结构。
Zα域InsideOutBio最初是由阿兰·赫伯特博士发现,在纸上一个通信作者。的ADAR1 Zα域关闭自身免疫反应,而其他ZBP1 Zα打开通路杀死病毒感染细胞正如前面所示的Sid Balachandran博士,其他作者在纸上交流。ADAR1之间的交互和ZBP1判断肿瘤细胞生命或死亡。
两个Zα被干扰素诱导蛋白在炎症。他们通常不出现在正常细胞。两种蛋白质也表达在肿瘤,特别是在正常细胞称为成纤维细胞癌症细胞力来支持他们的发展。通常情况下,依靠ADAR1抑制肿瘤细胞死亡通路,否则杀死肿瘤。
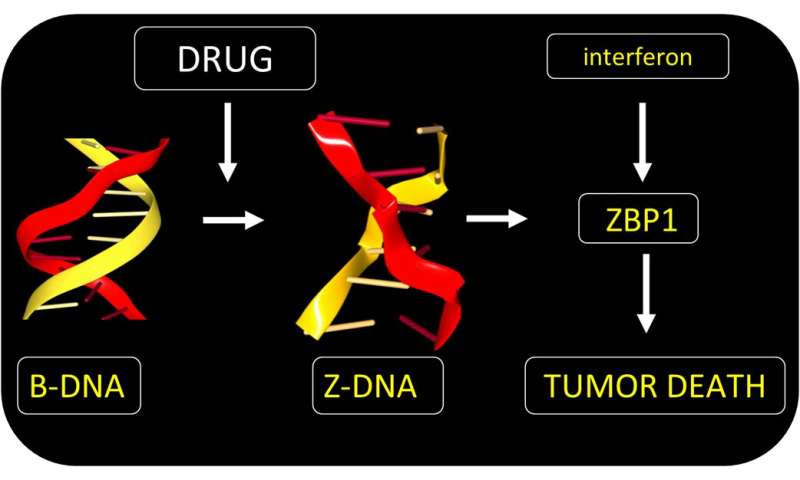
研究小组发现一个小分子,可以绕过ADAR1 ZBP1直接抑制和激活肿瘤细胞死亡。毒品行为无论突变导致癌症。细胞死亡的形式诱导免疫原性。破坏了成纤维细胞的响应支持肿瘤的生长。通过这样做,该药物增强免疫疗法的有效性使用针对PD-1 checkpoint-blocking抗体。该药物是curaxin家族的一员,被介绍给诊所为另一个目的。第一阶段试验化合物被证明是安全的,但仍需要进一步的研究来证实其临床使用结合anti-PD1提供了一个在癌症的治疗中获益。
赫伯特博士说:“这一结果是一个高度协作的团队的工作。我们理解这是一个不错的里程碑的替代DNA构象,像Z-DNA,扮演着重要的角色在人类生物学。本文展示了基础研究可能导致新的、意想不到的治疗。流程已经很长时间了,从最初的发现Zα域,然后确定ZαDNA变异导致人类遗传疾病。这些发现为Z-DNA验证生物作用。工作已经带领我们到一个新的治疗方法治疗癌症。取悦好转,考虑到初始Z-DNA发现被广泛被科学界的小生物的重要性和进一步工作没有列为值得资助的美国国立卫生研究院的同行评审小组”。
Z-DNA序列称为flipons形成于正常细胞,在生理条件下能可逆地翻转左撇子构象。结构是由事故发现首次合成晶体x射线晶体学来解决。其他类的flipons存在,也极有可能在生物学中发挥着重要作用。Flipons高度动态结构已经很难研究,因为它是具有挑战性的,以确定他们的确切的细胞内构象。赫伯特博士说,“这是类似于其他高度动态系统在物理你只能找到flipon构象进行直接测量,但前提是测量不偏见的行为的结果。”