过度的线粒体退化是正常的临界点酒精代谢酒精性肝病
虽然大多数通常被称为细胞的“强国”,因为他们的能源生产能力,线粒体也发挥重要的作用在调节细胞的健康。这些重要结构与人饮酒会损伤,这可能会导致他们破裂并释放DNA、蛋白质和脂质,统称为“损害相关的分子模式(抑制)。”
破裂线粒体和释放的抑制导致广泛的炎症,从而导致细胞损伤肝,导致肝脏疾病,甚至癌症。为了防止这样的情况发生,细胞这一过程被称为mitophagy移除受损的线粒体有选择地才引起炎症。然而,流程规范mitophagy及其对肝脏健康的长期影响酒精暴露条件所知甚少。
更全面了解酒精损害线粒体,以及这如何导致mitophagy,南卡罗来纳医科大学的研究人员(音乐)使用一个先进的成像技术探讨在小鼠的肝脏线粒体功能的变化,暴露于酒精。他们的发现,3月16日在线发表在《华尔街日报》自噬,表明暴露于酒精会导致一种特定类型的线粒体损伤称为去极化。在一个全新的发现,他们发现这个细胞去极化,表明线粒体受损,从而导致激活mitophagy机械移除受损的线粒体才能造成伤害。
“线粒体可以成为定时炸弹,我们必须包含它们,”约翰·j·Lemasters说,医学博士博士,中心主任细胞死亡、伤害和再生,葛兰素史克在药学院杰出赋予的职位。
以前,研究人员指出,急性(或短期)酒精exposure-such后,发生在一个晚上的狂欢drinking-mitochondria受损但可以恢复。在肝脏,酒精处理有毒分子乙醛(AcAld)产生,从而损害细胞。在移除AcAld线粒体援助,但他们已损坏或去极化的在这个过程中,需要删除。细胞的线粒体是复制,继续正常工作。
因此,Lemasters所总结的,他最初创造了这个词mitophagy,破坏的形式去极化是有益的,因为它有助于迅速除去乙醇,特别是有毒副产物乙醛。
然而,在慢性酒精exposure-such(或长期)条件的发生经过多年的酒精消费如酒精addiction-the线粒体损伤的不断循环其次是去除成为致病,减少健康线粒体仍然每一次。一致的很多受伤的线粒体导致线粒体消耗综合症等问题,在没有足够的ATP产生(或能量)。其他细胞功能也开始下降。
目前的研究认为线粒体损伤,特别是去极化,启动mitophagy防止受损的线粒体细胞中积累。阻塞乙醇暴露后去极化也块mitophagy,防止线粒体消耗。
“没有任何线粒体比坏线粒体,“Lemasters说。
这些所谓的“坏”线粒体毒性AcAld已经损坏,可以释放有毒抑制细胞如果不是隔离和退化。钟,医学博士博士,药物发现和生物医学科学系的教授和高级在这项研究中,作者提到,抑制可能是有用的在将来的研究中。
“线粒体抑制与肝细胞损伤和可以被用作生物标记看相关性疾病和肝损伤的严重程度,”钟说。
直接抑制去极化可能是困难的。因此,该小组调查方法协助线粒体处理AcAld以便减少线粒体是通过去极化和退化的受伤。一个方法是提高酶的活性处理AcAld使用一种名为Alda-1的药物。虽然这种药物治疗成功地减少了受伤的线粒体的数量在小鼠的肝脏,Alda-1在临床试验中显示重要广泛的毒性,因此一个贫穷的候选人供临床使用。然而,成功的Alda-1减少线粒体损伤,这可能是有益的从长远来看,发展更好的药物提供了依据和方法对预防肝线粒体损伤。
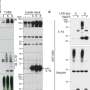
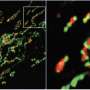
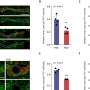
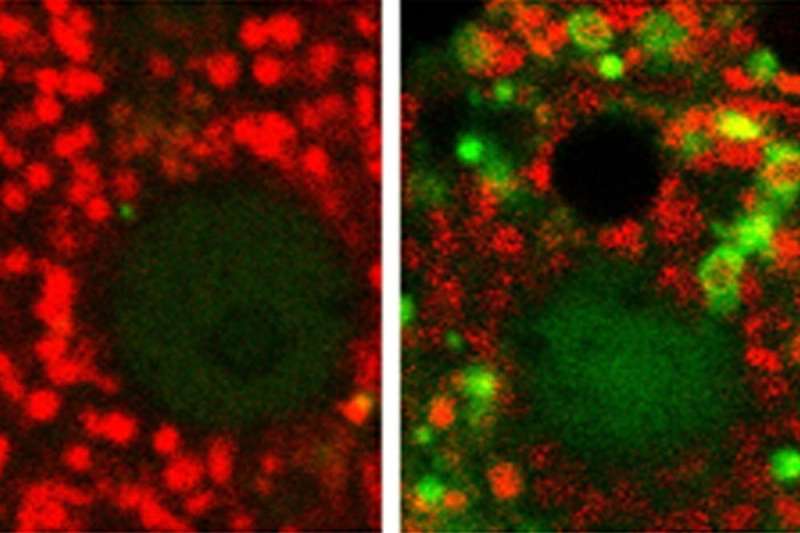
有趣的是,在这项研究中提出的问题只能回答使用动物模型。这是因为在细胞培养模型中,线粒体去极化后不发生急性酒精治疗。因此,研究人员使用一种相对较新的技术活体的多光子显微镜,这是一种奇特的方式获得活体动物的细胞结构的详细图像。结合创新的小鼠模型,使荧光颜色的电池组件,允许他们的健康和交互被追踪到,以前不能回答的问题关于酒精暴露在线粒体的后果。
音乐团队能够确定这两个急性和慢性酒精暴露导致线粒体损伤的形式去极化。线粒体去极化直接启动mitophagy降解受损的线粒体。而急性损伤可以通过复制的健康和损伤修复线粒体,慢性暴露于酒精会导致重复线粒体退化,导致线粒体消耗,炎症、肝纤维化、肝硬化,最终,肝脏疾病。
确定酒精损害线粒体可能导致早期肝脏疾病诊断的新方法和开发更有效的治疗。以及提供更详细的基础科学知识的线粒体功能和触发的mitophagy,这手稿奠定了基础为未来的研究开发新型治疗酒精和不含酒精的肝脏疾病。