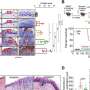
鼻咽癌治疗使用液细胞来源于γδ-T主体性与放射治疗
路医学院研究小组,香港大学(HKUMed)发现液源自γδ-T细胞(γδ-T-Exos)主体性与放射治疗可以控制鼻咽癌(NPC)克服人大癌症干细胞的抗辐射性(二者)和保存他们tumor-killing和T cell-promoting人大免疫抑制微环境的活动。本研究为小说提供了一个概念验证和强有力的战略结合γδ-T-Exos NPC放射治疗在控制。研究结果已发表在杂志对癌症免疫疗法。
鼻咽癌(NPC)是一个最激进的eb病毒(EBV)相关的肿瘤,在东亚地区非常普遍,包括香港。放射治疗是人大的一线治疗,但其治疗效果差一些病人由于抗辐射性。基于T细胞过继免疫治疗也显示承诺控制人大;然而,它的抗肿瘤功效可能减毒的免疫抑制肿瘤微环境。细胞外液endosome-originated小泡,调节细胞间的沟通。与细胞疗法相比,液游离与更高的安全优势,更容易储存和降低成本。在先前的研究中,研究人员已经证明,γδ-T-Exos可以有效地控制EBV-associated肿瘤的进展。然而,它仍然未知γδ-T-Exos是否有协同效应与放疗和保持其抗肿瘤活动对人大的免疫抑制肿瘤微环境。
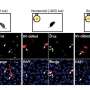
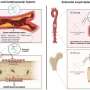
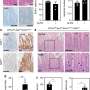
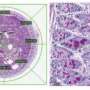
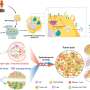
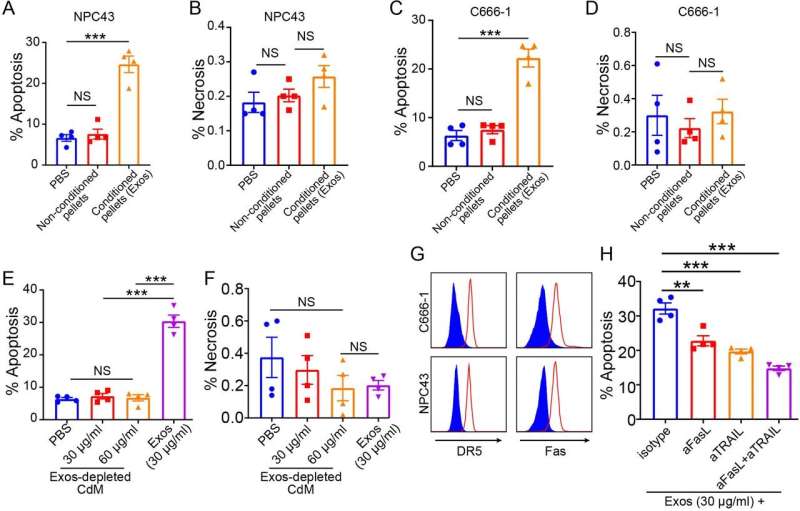
研究小组发现,γδ-T-Exos不仅有效地与人大细胞和体外诱导肿瘤细胞死亡,这主要是由Fas / Fas配体(FasL)和死亡受体5 (DR5) /肿瘤坏死factor-related凋亡诱导配体(TRAIL)途径,而且人大控制肿瘤的生长和延长肿瘤小鼠体内生存。此外,γδ-T-Exos选择性地靶向抗放射性的CD44 + /高二者和诱导的细胞凋亡。的组合γδ-T-Exos CD44 + /放射治疗克服了抗辐射性高NPC细胞,显著提高其治疗效果对人大在体外和体内。此外,γδ-T-Exos提升T细胞迁移到人大肿瘤移植CCR5在T细胞被CCR5 chemoattracted配体在全国人大肿瘤微环境。虽然人大肿瘤细胞分泌丰富的肿瘤生长因子β(TGF-β)抑制T -细胞反应,γδ-T-Exos保存直接抗肿瘤活动和克服了免疫抑制人大增强T细胞抗肿瘤免疫微环境。
“我们的研究首次提供了一个强有力的临床前概念证明使用一种新颖的治疗策略,γδ-T-Exos结合放疗治疗人大。γδ-T-Exos可以有效地相互作用和杀死EBV阳性和阴性NPC细胞。更重要的是,γδ-T-Exos可以消除抗放射性的人大二者和保存他们tumor-killing和T cell-promoting人大免疫抑制微环境的活动。因此,结合放疗与γδ-T挂式在人大的治疗潜力巨大,这将非常有利于临床应用这种方法,”教授说你Wenwei系的儿科和青少年医学,临床医学学院HKUMed,谁领导了这项研究。ob体育开户网址
这项研究的意义
这个研究的发现在癌症免疫治疗有着重要的意义。首先,γδ-T-Exos和CD44 + /互动高人大二者高功效。因此,γδ-T-Exos可以补充放射治疗,加强对人大的治疗效果。其次,γδ-T-Exos优于其他exosome-based疗法结合电离辐照在NPC治疗(例如MSC-Exos)保持抗肿瘤免疫抑制人大微环境的活动,更容易准备。第三,结果γδ-T-Exos扩展已存在的肿瘤特异性T细胞的免疫抑制人大微环境可以大大提高γδ-T-Exos的临床可行性。因此,它是重要的联合治疗拥有免疫刺激性影响增强抗肿瘤免疫的免疫抑制微环境。