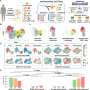
遥控CAR-T细胞疗法更安全,在小鼠研究中更有效
根据小鼠最近出版的一项在小鼠中发表的一项研究,一种使用患者自己的转基因免疫细胞攻击癌细胞的癌症治疗方法更安全,更有效。
原始疗法被称为CAR-T细胞疗法,对某些类型的血液癌非常有效。但是,因为某些患者对工程细胞,通常仅在尝试其他治疗后才使用CAR-T疗法。
在实体瘤患者(例如脑和骨癌患者)中,它也不太成功。研究人员认为,这是因为在消除实体瘤之前,容易产生过多信号传导的CAR-T细胞会筋疲力尽。此外,与血液癌不同,很难鉴定仅在实体瘤上发现的分子靶标的癌细胞而不是在正常组织上。
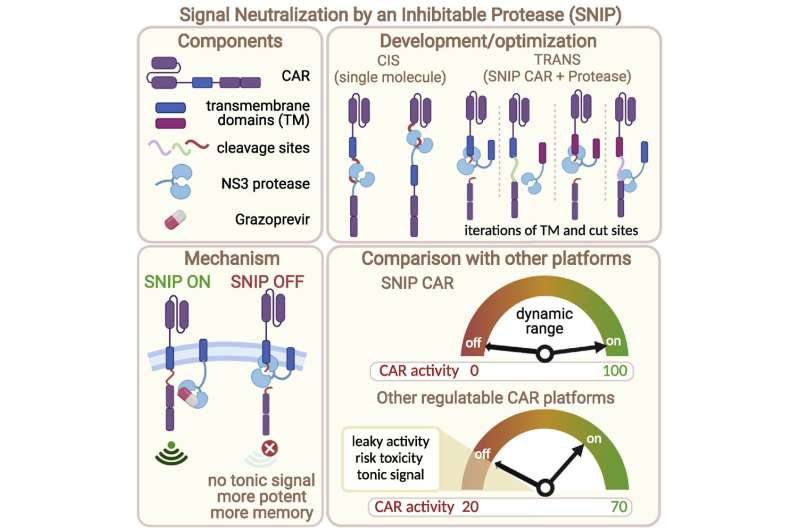
斯坦福大学的研究人员设计了一种修改后的CAR-T细胞疗法,称为SNIP CAR-T,该疗法被食品药品监督管理局已经批准用于人类使用的肝炎的口服药物。(没有药物,剪切CAR-T细胞不活跃。)
将细胞的活性控制在患者中后,用药物控制细胞活性的能力为那些可能对转基因细胞反应不佳的人提供了一种安全机制。研究人员还发现,修饰的CAR-T细胞在应对固体癌症方面的有效性明显更高实验室小鼠- 可能是因为细胞经历了短暂的,重复的休息时间,因为每天的药物在动物的身体中被代谢。
“我们创建了一种'遥控'CAR-T疗法,可为每个患者进行调整,” MD Crystal Mackall,Ernest和Amelia Gallo家庭教授,儿科和医学教授。ob体育开户网址“这些改良的CAR-T细胞不仅更安全,而且比原始的CAR-T细胞更有效,更具用途。这是一个非常复杂的系统。”
Mackall是该研究的高级作者,该研究于4月27日在线发布细胞。研究生Louai Labanieh是该研究的主要作者。
Labanieh说:“我对snip car-t细胞比常规CAR-T疗法更好的程度感到惊讶。”“在常规CAR-T完全失败的情况神经系统。”
因为口服药物这触发了SNIP CAR-T细胞的活性已得到FDA的批准,研究人员希望在未来24个月内对患有实体瘤的人进行临床试验。
使免疫细胞起作用
CAR-T细胞由免疫细胞称为从患者中收集并在实验室进行基因设计的T细胞,以识别和攻击其表面上特定分子的癌细胞。然后,他们被注入患者与疾病作斗争。当CAR-T细胞上的受体与癌细胞上的靶标结合时,它在CAR-T细胞内启动了链反应,该链反应信号以杀死癌细胞。
CAR-T细胞疗法首先被FDA于2017年批准用于儿童和年轻人与急性淋巴细胞白血病。从那时起,它也被批准用于其他血液癌的成年人,包括多种骨髓瘤和几种类型的淋巴瘤。该治疗的原始形式靶向一个称为CD19的癌细胞表面的分子,但研究人员还在测试识别其他分子或两个分子靶标而不是一个分子的CAR-T细胞。
Labanieh希望开发一个CAR-T系统,该系统可以在将细胞返回给患者后很容易控制。他在称为蛋白酶的CAR-T细胞中引入了病毒蛋白。该蛋白酶切断了细胞膜内侧的CAR-T受体,阻塞了触发细胞杀伤活性的信号传导级联反应。蛋白酶可以被称为Grazoprevir的药物灭活,该药物被批准用于治疗丙型肝炎。在没有药物的情况下,细胞不活跃。当存在药物时,细胞开始杀死癌细胞。
Labanieh和他的同事表明,在没有Grazoprevir的情况下,SNIP CAR-T细胞在实验室小鼠中无活性。相反,当给小鼠口服格拉索氏菌时,抑制蛋白酶并激活剪切CAR-T细胞。在CAR-T诱导的致死毒性的小鼠模型中,在格拉Zoprevir治疗停止后通过snip CAR-T细胞进行治疗的小鼠停止了,这证明了该系统的潜力比常规CAR-T疗法更安全。
Labanieh说:“以前的创建药物调节的CAR-T细胞的努力已经产生了非常挑剔或漏水的系统。”“这是我们第一次能够如此精确地调整他们的活动。”
Mackall补充说:“当带有全剂量grazoprevir的剪裁CAR-T系统启动时,它已经亮起。”“当格拉索普雷维尔(Grazoprevir)消失时,它已经关闭。这对于经历毒性的患者至关重要。我们可以关闭细胞并给患者恢复时间。大多数其他安全开关旨在杀死CAR-T细胞或对永远关闭它们。患者可能会在治疗中幸存下来,但仍无法治愈癌症。”
靶向实体瘤
当研究人员测试了剪切CAR-T细胞在小鼠中与固体癌作斗争的能力时,他们发现它们比传统的CAR-T疗法更有效 - 在许多情况下,用称为髓母细胞瘤或骨骼的脑癌固化小鼠癌症称为骨肉瘤。
出乎意料的是,他们还发现,调节grazoprevir剂量使CAR-T细胞更加敏感,将其杀伤活性集中在具有较高靶分子的癌细胞上,同时保留同一分子水平较低的正常组织。能够设计CAR-T细胞识别靶标分子的能力健康细胞可以改变应对人类的能力实体瘤研究人员说。
麦克尔说:“这是一种非常有吸引力的可能性。”“如果仅通过更改格拉Zoprevir的剂量来降低SNIP CAR-T细胞的活性,我们就可以非常精确地对每位患者进行个性化疗法,防止毒性或驱动CAR-T细胞在正常组织上杀死癌细胞。我们认为这是一种下一代癌症疗法,它将改变CAR-T细胞场。”
进一步探索