早期乳腺癌的乳房导管治疗消除了实验室实验中所有疾病的迹象
通过乳头中的开口将有靶的免疫毒素传递到乳房导管中,在实验室研究中消除了所有可见且看不见的癌前病变,由非常早期乳腺癌的Johns Hopkins Kimmel癌症中心的研究人员领导。
对小鼠进行的工作的描述,作者说,这为有0期乳腺癌的患者进行可行性和安全试验提供了强大的临床前基础,并于6月8日发行美国国家科学院论文集。
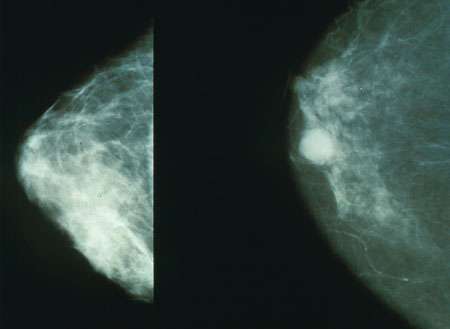
阶段0乳房癌症,也称为导管癌原位(DCIS)的特征是异常的存在癌前细胞乳房内的牛奶管道,在美国每年影响约69,000名妇女。约翰·霍普金斯肿瘤学和病理学教授约翰·霍普金斯(Johns Hopkins)教授,许多妇女对这些早期的癌症进行了乳房清除手术和放射治疗,在某些情况下,她们接受了化学疗法或激素疗法。
Sukumar说:“在我们的研究中,我们提出了一种替代治疗方法,其中通过管道注射免疫毒素药物可能会导致DCIS清理。”“令我们惊讶的是,这些毒品杀死了那个乳房管道中存在的每一个病变。我一生中从未见过如此戏剧性的结果。”
在研究过程中,研究人员首先评估了靶向免疫毒素HB21(FV)-PE40的细胞杀伤作用,在不同的分子亚型的四个细胞系中乳腺癌。毒素由HB21(一种单克隆抗体)组成,一种可以与特定靶靶结合的蛋白(在这种情况下,与人类转铁蛋白受体(在乳腺癌中发现的载体蛋白)组成。HB21与PE40融合,PE40是细菌毒素的片段,该毒素停止了细胞中的蛋白质产生并导致细胞死亡。结果表明,该治疗诱导所有细胞系中强烈的杀伤性作用。研究人员还对约10只小鼠进行了治疗,以寻找治疗后血液中循环的毒素,并在注射后五到30分钟发现毒素没有。
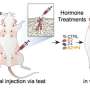
接下来,他们将HB21(FV)-PE40注入了两种小鼠DCIS:MCF7和SUM225的小鼠模型的乳房管道。在MCF7小鼠中,该治疗每周一次进行三周。处理非侵入性成像的处理。为了比较,他们还将治疗剂施用到体内,并将HB21抗体单独递送到某些小鼠的管道中。这两个模型代表了人类乳腺癌常见类型的所有分类:雌激素和孕酮受体阳性和人表皮生长因子受体2(HER2)阴性,雌激素和孕激素受体阴性和HER2阳性。
在MCF7模型中,在体内接受毒素治疗的人的肿瘤生长较慢。然而,肿瘤在第26天左右停止治疗后复发。另一方面,在通过管道接受治疗的模型中,肿瘤在完成三种治疗中的两次后的两周内消失了,并且甚至通过成像也没有复发。61天后。
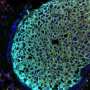
在第32天,研究人员对每组两组进行了乳腺的病理检查。他们发现肿瘤细胞不存在,并且该体系结构与正常的乳腺一致。在61天后对其余样品的类似分析显示,在仅接受HB21的模型中,在体腔中接受的小肿瘤,在通过管道接受毒素治疗的患者中没有肿瘤。
在SUM225模型中,对毒素处理的试验实验最早在两周的治疗中显示出肿瘤的清除,如通过成像所见。直到在第48天终止实验之前,才观察到复发性。全管内治疗后,大多数乳腺是无肿瘤的,剂量较低的作用较弱。发现SUM225肿瘤在导管位置积极生长。病理研究表明,仅HB21抗体几乎没有作用,而免疫毒素结合治疗对肿瘤减少的影响显着影响。
治疗良好,没有毒素或注射的副作用。
由于大多数低级DCI都不会进行,因此主动监视和激素疗法Sukumar说,建议使用更大的病变治疗。她说:“这种较大的高级DCI可能是损伤的病变,在这种病变上,内内灌输免疫毒素是最有益的。”最大的优点是,通过导管内途径进行免疫毒素使其能够达到导管树中的所有癌症病变,甚至消除了那些通过成像乳房不可见的癌症。
Sukumar说:“可能的临床研究看起来像这样。”“手术前一两个星期,研究人员可以通过单个管道通过低剂量的HB21(FV)-PE40来给女性使用,并慢慢使用增加剂量来确定是否有任何免疫毒素将管道逃脱到血液中并影响肝功能。它们也会影响肝功能。它们也会影响肝脏功能。它们也会逃脱。会检查管道之后胸部去除以寻找组织的变化及其对癌前病变的影响。”
研究的合着者是约翰·霍普金斯(Johns Hopkins)的Guannan Wang,Alok Kumar,Preethi Korangath,Priya Pai和Kathleen Gabrielson;中国武汉大学的金融医院的Wanjun丁;国家癌症研究所的塔潘·贝拉(Tapan Bera),朱西亚·韦(Junxia Wei)和伊拉·巴德坦(Ira Pastan)。
进一步探索