深度学习能够发现癌症中新的基因突变
根据《杂志》上发表的一项研究科学进步。
这些发现为癌症据Feng Yue博士说,分类和潜在疗法,杜安(Duane)和苏珊·伯纳姆(Susan Burnham)分子医学教授兼研究高级作者。
“我们的工作确定了许多以前未知的融合事件癌症基因组还捕获了已知的癌基因的新型调节机制。
在每个细胞中,需要精确地折叠和组织长的DNA链,以便它们可以安装在细胞核内,这通常只有几微米的直径。以前,Yue和他的合作者表明结构变体在癌症基因组中,例如反转或易位,可以在基因组分析工具(例如HI-C)中检测到。
这些模式可以通过计算机算法识别为结构变化的指标。此外,根据Yue的说法,这些较大的结构变化通常被整个基因组测序(WGS)丢失,甚至长期读取了纳米孔等长读取测序。
Yue说:“ WGS非常擅长检测基对突变和短插入或缺失,但很难检测到更大的变化。”

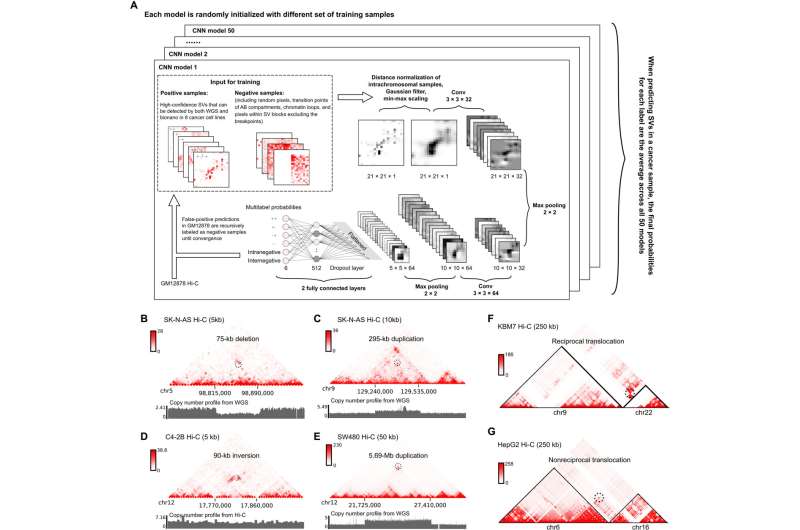
在这项研究中,Yue和他的合作者从八种癌细胞系中收集了一组不同类型的策划的高信心结构变化。这些被用来训练A深度学习模型- 名称为EAGLEC - 学习埋在这些信号中的隐藏模式。结果通常与传统的基因组测序技术一致,WGS或纳米孔测序也发现了70%至80%的基因组变异。
但是,EAGLEC发现了数百个其他融合事件,这些事件被全基因组测序或长阅读测序遗漏。根据Yue的说法,这些新发现的事件代表了HI-C检测到的总遗传变异的10%至20%。
这些融合事件中有许多导致癌基因与通常位于另一个染色体上的远端增强剂之间的联系。这些事件称为“增强剂 - 爆炸”,可能导致癌基因的上调。
在研究中,研究人员使用EAGLEC搜索100多个以上的结构变化癌细胞系和患者样品,发现其他基因组测序可能会遗漏的其他融合事件。根据Yu的说法,使用这种模型可以扩大对结构变异的知识及其对癌症相关基因的影响。这可能在前列腺和乳腺癌,两个最常见的癌症也具有很高的融合事件。
Yue说:“我们可以看到在没有融合事件的癌症和没有癌症的癌症的治疗反应中是否存在差异。”“我们的发现还为癌症研究人员提供了许多控制基本癌基因和途径的新型调节剂。”
EAGLEC也可用于检测单细胞HI-C分析中的结构变化,其中数据很少。这使科学家可以检查单个癌细胞之间的异质性。
Yue将来说,他希望将此模型应用于更多的癌症样本,并寻找针对新的潜在药物融合在当前研究中发现的事件。
进一步探索