全基因组癌症抑制剂的错综复杂解开
发表在《西北医学》杂志上的一项研究表明,一种新发现的常见致癌蛋白抑制剂有选择性地起作用,减少了促进细胞疯狂增殖并改变表观基因组的基因表达科学的进步.
据妇产科安娜拉帕姆教授、妇产科转化研究副主任、该研究的共同高级作者Debabrata Chakravarti博士说,这种名为MYC的蛋白质以前被认为是“不耐药的”,但这些新发现表明,某些抑制剂可能会选择性地影响促癌过程。
“这些发现为构建和测试用于MYC抑制的所有新化合物系列奠定了基础,”Chakravarti说,他也是西北大学Robert H. Lurie综合癌症中心的药理学教授和共享资源助理主任。
MYC是一种通常上调的转录因子蛋白基因参与细胞增殖.该转录因子在许多癌症中持续高表达,但由于该蛋白不寻常的结构及其在细胞增殖之外的巨大影响,设计抑制剂非常复杂,这意味着之前的抑制剂有严重的毒副作用。
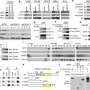
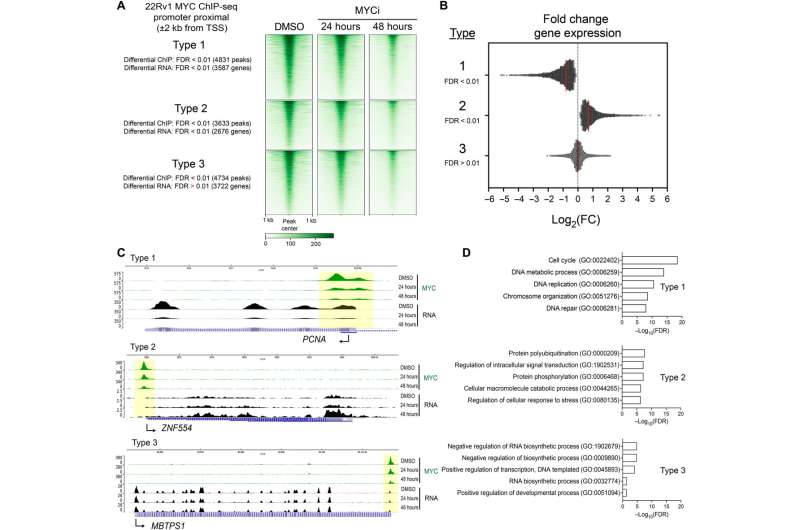
在目前的研究中,研究人员将一种名为MYCi975的小分子抑制剂应用于前列腺癌细胞,研究其对基因表达整个人类基因组。出乎意料的是,MYCi抑制剂并没有广泛下调所有MYC靶点,而是具有不同的效果——上调某些基因,下调其他基因,以及完全保留一些基因。
“这是我们收集关于药物选择性信息的方法,”奥斯丁·霍姆斯说,他是Driskill生命科学研究生项目(DGP)的应届毕业生,也是该研究的主要作者。
重要的是,根据Sarki Abdulkadir医学博士,泌尿学研究教授,泌尿系研究副主席和该研究的共同高级作者John T. Grayhack医学博士的说法,一些对细胞功能至关重要的基因——可能是先前MYC抑制剂毒性的原因——没有受到影响。
“不是所有的MYC功能都被废除了,”Abdulkadir说,他也是病理学教授和卓越研究专业计划(SPORE)的首席研究员前列腺癌卢瑞癌症中心“这给了我们一些以前没有表现出来的选择性。”
另一方面,MYC的几个与癌症相关的靶点被下调,保持了抑制剂的抗癌效果。认识到MYC抑制剂可以对MYC下游基因靶点发挥可变作用,为未来的研究提供了新的途径药物开发据查克拉瓦提说。
“令人兴奋的是,在动物模型中,MYCi975增强了enzalutamide抗激素治疗的疗效。我们希望利用这个平台来分析第二代或第三代化合物,并探索这些药物如何与现有的抗癌疗法相互作用,”Chakravarti说。“这项研究也是合作研究如何在生物医学研究中产生重大发现的一个原型。”ob欧宝直播nba