研究人员展示了肝脏如何控制大脑和行为
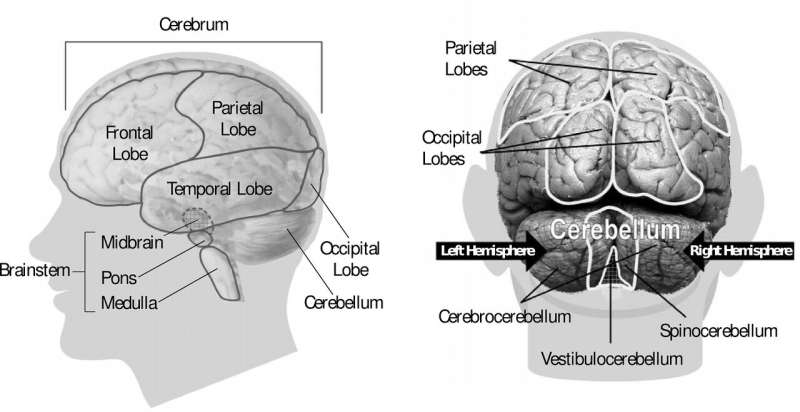
耶鲁大学的一项新研究发现,肝脏在调节小鼠的进食行为方面起着重要作用,这一发现可能会对饮食失调和代谢疾病患者产生影响。这项研究是与德国同事合作完成的,也增加了越来越多的证据,表明大脑最高级的部分——大脑皮层会受到身体其他部分的影响,而不是相反。
“这项工作的一个结论是,试图通过只观察大脑本身来理解大脑功能的经典方法并不能给你完整的画面,”耶鲁大学医学院的珍和大卫W.华莱士比较医学教授Tamas Horvath说,他是这项研究的资深作者,于6月27日发表在《柳叶刀》上自然的新陈代谢.
在一系列实验中,研究小组发现了大脑和肝脏相互交流和控制的电路。这一对话的两个关键参与者是一组被称为AgRP神经元的细胞,它们存在于大脑的下丘脑区域,以及一种由肝脏分泌的脂质,称为溶血磷脂酰胆碱(LPC)。
AgRP神经元,与大脑皮层大脑皮层是大脑的外层,与复杂的行为和能力有关,对于促进情感的发展至关重要饥饿.但它们也与身体的其他部位交流,比如肝脏和胰腺;当人类饥饿时,这些神经元在从体内储存的脂肪中释放脂质方面起着关键作用。
一旦LPC被肝脏分泌,血液中的一种酶会迅速将其转化为溶血磷脂酸(LPA)。其他研究人员已经证明LPA可以改变大脑中的神经元活动。
在这项研究中,研究人员观察到,禁食后,小鼠血液和脑脊液(中枢神经系统内发现的特殊液体)中的LPA水平都有所提高。LPA水平的上升引起了皮层神经元活动的增加,这引发了禁食后食欲的增强。所有这些效应都依赖于AgRP神经元的功能。
这些发现表明AgRP神经元调节肝脏和脂质释放后,这些脂质会循环回大脑,影响大脑皮层及其功能。
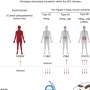
霍瓦特说,还需要更多的研究来确定人类是否存在类似的回路,但他和他的同事确实发现了一些证据。经历突变导致更大的lpa诱导的神经元活动的小鼠比典型的小鼠吃得更多,体重更重。与没有这种基因突变的人相比,携带这种基因突变的人往往有更高的体重指数和更高的2型糖尿病患病率。
霍瓦特说:“我们仍然需要更严格地探索这些机制是否与人类相关,但如果是的话,我们就可以开始研究我们是否可以利用这些机制来治疗饮食失调和其他疾病。”“但这表明肝是行为的主要驱动因素。这增加了停留在大脑中来理解大脑这还不够。”
这项研究的其他耶鲁作者有Bernardo Stutz、Zhong-Wu Liu和Matija Sestan-Pesa。
进一步探索