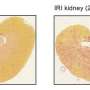
研究人员模拟冠状病毒感染人类肺部和瀑样使用
全球研究人员继续努力改善我们的理解机制COVID-19感染和肺炎和肺损伤偶尔与之关联。作为这些努力的一部分,研究人员从查利特,柏林健康研究所的查利特(波黑)、马克斯·德尔布吕克分子医学中心(MDC)罗伯特·科赫研究所和柏林自由大学的传播进行了分析,和免疫激活,SARS-CoV-2病毒在人类肺部。具体地说,研究人员专注于肺泡内的细胞和肺泡巨噬细胞。后者是吞噬细胞的先天免疫系统清理肺部摄取和消除外国粒子,包括感染性病原体如病毒和细菌。
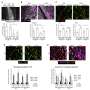
Andreas Hocke博士教授领导的查利特的传染病和呼吸医学的研究团队发现,SARS-CoV-2感染的很少上皮细胞衬里肺泡表面,这意味着它会导致很少直接组织损伤。在这方面,该病毒不同显著MERS-CoV和流感病毒。通过综合光谱microscopy-based分析,研究者还可以显示只有很少的肺泡上皮细胞拥有ACE2受体,由SARS-CoV-2需要获得进入宿主细胞。
“使用人类的肺和肺organoids-models人类肺泡的开发使用干细胞收获从人类肺组织我们能够表明SARS-CoV-2直接依赖于它的受体。通过这样做,我们可以排除其他替代受体,”该研究的第一作者解释说,博士Katja Honzke查利特的传染病和呼吸道医学系。
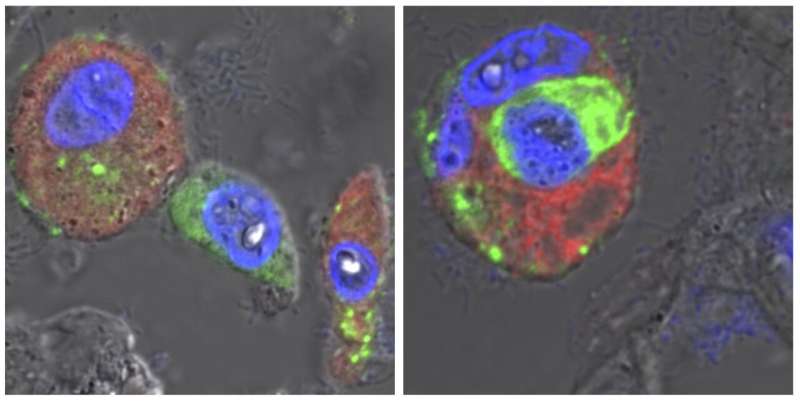
当大量的SARS-CoV-2到达肺泡上呼吸道,这些不肺内广泛传播的上皮细胞,通常情况下在其他严重的病毒感染。相反,他们通过巨噬细胞摄取。
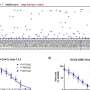
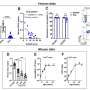
“使用详细的生物信息学分析和COVID-19尸检样本,我们观察到巨噬细胞改变摄取冠状病毒后,“co-first作者波黑的Benedikt Obermayer-Wasserscheid博士说。这些变化反过来又引发一系列的反应与肺炎。巨噬细胞释放炎性使者和偶尔会引发严重的炎症级联。研究人员还发现,不复制这些免疫细胞内的病毒。
解释研究结果,Hocke教授说:“我们的研究表明,严重肺损伤COVID-19更可能是由于macrophage-induced免疫激活比直接损害肺泡占据。因此,它对我们理解疾病进展作出了重大贡献在早期阶段的潜在COVID-19肺炎和显示原因,相比之下,即冠状病毒,大多数情况下SARS-CoV-2感染相对温和的疾病严重程度。”
因此安全假设,在大多数情况下SARS-CoV-2感染,局部免疫机制在人类肺组织有效地清除病毒和限制炎性反应。这个不能happen-something可能受到个人因素:感染风险的影响,在极少数情况下,证明严重甚至致命。Hocke教授继续说:“我们使用的肺模型提供了一个很好的例子的人类细胞替代动物模型是特别有用的人畜共患疾病的研究。我们能够这样做由于我们与查利特3 r的密切合作,一个设施,致力于发展替代动物性的研究。”
这项研究发表在了欧洲呼吸杂志。后续研究将着眼于patient-derived瀑样模型,它将被用于更详细研究的一般风险因素如年龄、性别、伴随疾病和不同的药物影响免疫反应的激活。这些知识可能会使可能的治疗方法针对免疫系统的识别。