心力衰竭的单细胞图表明可能的治疗靶标
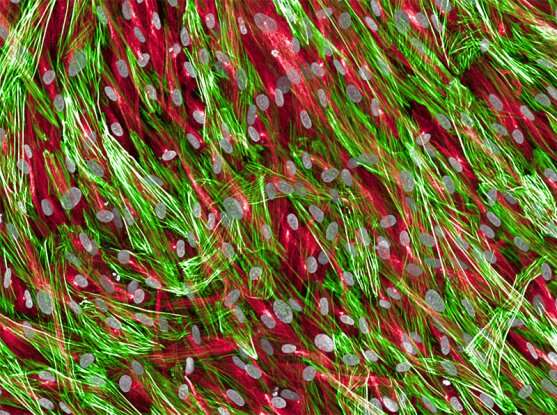
麻省理工学院和哈佛大学和拜耳的Precision心脏病学实验室(PCL)的科学家生成了心脏中各种细胞类型的详细地图,这些地图涉及两种主要的心力衰竭原因:扩张和肥厚的心肌病(DCM和DCM和DCM和HCM),两者都损害了心脏的抽水能力。
该团队的发现今天在自然,建议可以针对新治疗的特定细胞类型和生物学机制。心力衰竭是美国最常见的住院原因之一。现有药物有限,许多患者最终死于心脏衰竭。
为了创建其细胞图,研究人员使用了单核RNA测序(RNA-SEQ),该测序揭示了哪些基因是活性的,并且在单个细胞中的哪些水平。他们学习了心来自晚期心力衰竭患者的组织,发现DCM和HCM心脏细胞表达的基因不同于非失败心脏,但是DCM和HCM患者的基因表达谱相似。一些心肌病患者还具有独特的成纤维细胞或结缔组织细胞,研究人员认为可以有助于心力衰竭的组织疤痕,并且可能是将来治疗的目标。
这项研究以先前的努力为基于健康人心脏中的单个细胞进行分类,并且是与宾夕法尼亚大学医学和心力衰竭医师教授Ken Margulies紧密合作的结果。绘制涉及不同心力衰竭形式的细胞可以帮助研究人员识别标记,使它们能够区分疾病类型并预测临床结局。
帕特里克·埃利诺尔(Patrick Ellinor)说:“目前,几乎所有形式的心力衰竭都类似地对待。”,以及哈佛医学院的教授。“我们的目标是在疾病患者中询问健康和疾病之间有不同的细胞群体或基因?是的,我们发现在某些疾病患者中发现表明高活性心脏成纤维细胞的基因。”
“拜耳和广泛的科学家并排工作,以生成,分析和验证这项研究的数据。学术界与学术界之间的合作水平制药行业非常罕见,”拜耳和广阔的联合精密心脏病学实验室高级主管兼负责人卡拉·克拉滕霍夫(Carla Klattenhoff)说。“这张地图是心脏病学领域的惊人资源。”
拜耳(Bayer)治疗区1负责人乌尔里希·尼尔斯(Ulrich Nielsch)补充说:“这是加深对疾病的理解,为加深我们对疾病的理解做出的重要科学贡献。”
通过细胞
先前的研究发现,失败的心脏具有独特基因表达谱与健康的心脏相比,或转录组相比,这项工作仅产生了整个心脏的单个遗传指纹。相比之下,使用单核RNA-Seq,Ellinor的团队使用了计算方法按细胞类型分开转录特征。这也使他们能够拾取稀有细胞类型的签名,这些稀有细胞类型可能在批量分析中被淹没了。
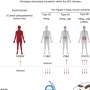
在他们的研究中,科学家们研究了DCM和HCM,这些DCM和HCM以不同的方式导致心力衰竭。在DCM中,心脏的左心室扩张,其墙壁稀薄,在HCM中,心脏的壁变得更硬,更厚。令他们惊讶的是,研究人员发现,尽管存在这些差异,但这些条件具有相同的转录指纹。通过进一步的研究,这一发现可以帮助医生更好地确定心力衰竭的形式和阶段相似,哪些形式和阶段相似,并且相应地进行了微调治疗。
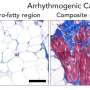
Ellinor的团队还发现,心肌病和健康患者之间的某些心脏细胞类型的丰富度有所不同。失败的心脏的肌肉细胞较少,但成纤维细胞比非击败心脏更多,这可能表明存在疤痕组织。在这些成纤维细胞中,研究人员还发现了只有失败的心脏中的独特人群。这项研究的广泛和第一作者的计算科学家马克·查芬(Mark Chaffin)说:“这对我们来说真是有多具体。”“心肌病心脏中有成千上万的核,而在非灭绝心中几乎没有。”
该团队使用CRISPR屏幕研究了关键基因的功能,该基因将成纤维细胞种群与正常心脏成纤维细胞区分开。他们发现,对于心脏成纤维细胞从休眠状态过渡到活跃状态,需要几个基因,在这种状态下,细胞形成可能阻碍心脏泵送的疤痕组织。查芬说,这些基因可能是未来治疗慢性疤痕组织形成或纤维化的可能靶标。
将来,研究人员希望通过寻找某些类型的成纤维细胞的迹象或心脏中较高水平的疤痕来找到一种方法来检测患者最早的心力衰竭。为了实现这一目标,该团队已经开始研究他们是否可以检测到血液中活化成纤维细胞的标记。
进一步探索