抑制念珠菌:抑制真菌感染的细胞
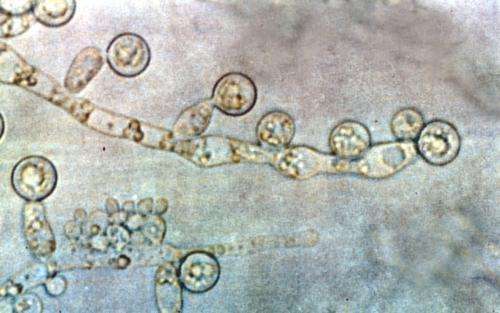
在生活在人体内的所有真菌中,最臭名昭著的可能是酵母菌念珠菌。这种面包酵母的远亲因引起各种类型的鹅口疮而臭名昭著,这可能是一个主要的麻烦,但它也可能导致侵入性感染,有时可能是致命的。今天发表在自然免疫学艾布拉姆松(Jakub Abramson)教授领导的魏茨曼科学研究所(Weizmann Institute of Science)研究小组发现了免疫系统在对抗念珠菌感染时使用的一种以前未知的防御机制。
假丝酵母菌在大多数健康人体内的含量都很低,它是微生物群的一部分——一种平静地生活在我们肠道和皮肤上的不同微生物谱。在正常情况下,假丝酵母菌会受到免疫系统的控制,但它偶尔会过度生长,侵入口腔粘膜、阴道、皮肤或身体的其他部位。在严重的情况下,它可以传播到血液,并从那里到肾脏。这种威胁生命的感染可能发生在一个人的免疫系统被削弱的时候,例如,艾滋病或免疫抑制药物,如癌症化疗或类固醇。抗生素可以消灭我们微生物群中的许多有益细菌,也可以通过提供酵母菌相对于-à-vis其他微生物的不公平优势,释放局部或侵入性念珠菌爆发。这就是为什么女性在服用抗生素后有时会患上阴道酵母菌感染。
直到现在,免疫细胞保护人体免受念珠菌侵袭的主要是T细胞类型的小而圆的淋巴细胞,称为T细胞H17.当防御失败时,这些细胞也要承担责任。
在这项新研究中,博士后扬·多贝斯科博士与魏茨曼免疫与再生生物系阿布拉姆森实验室的同事们一起工作,发现TH17个有战斗力的细胞假丝酵母如果没有一个完全不同的群体的关键早期支持,就无法产生:一个罕见的淋巴样细胞子集,称为3型先天淋巴样细胞(ILC3),它表达一种名为自身免疫调节因子(Aire)的基因
这两组细胞属于免疫系统的两个不同分支,它们就像徒步巡逻队和专门部队一样,联合起来对抗共同的敌人。air - ilc3是更古老的先天手臂的一部分,在遇到威胁时几乎立即行动起来——在这种情况下,是念珠菌感染。TH17s属于免疫系统较新的适应性臂,它需要几天甚至几周的时间来做出反应,但它发起的攻击比先天的更有针对性、更有力。
科学家们发现,一旦念珠菌开始感染组织,air - ilc3就会整个吞噬酵母,将其切碎,并在其表面显示一些酵母片段。这就是这些位是如何呈现给T音的H17s,其中一些通常在淋巴结待命,准备好感染警报。这种呈现方式指示专门的T细胞开始迅速分裂,数量从几个单独的突击队飙升到数百甚至数千个念珠菌特异性战士,能够摧毁感染部位的酵母。
“我们已经发现了以前未被发现的免疫系统这是有效对抗真菌不可或缺的武器感染,”艾布拉姆森说。
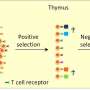
阿布拉姆松之所以对念珠菌产生兴趣,是因为它通常会导致Aire基因缺陷引起的罕见自身免疫综合征患者严重的慢性感染。艾布拉姆森的实验室对该基因进行了广泛的研究,帮助阐明它在预防自身免疫疾病中的作用。这项研究以及其他科学家的研究都表明,胸腺中表达air的细胞会指示发育中的T细胞避免攻击身体自身的组织。当Aire缺陷时,T细胞无法接受适当的指令,从而导致广泛的自身免疫,对身体多个器官造成严重破坏。但仍有一个困惑:为什么患有破坏性自身免疫综合征的空气缺乏患者也会发展成慢性念珠菌感染?
在试图完成Aire谜题的过程中,多贝斯科和同事们发现,在胸腺外,Aire也在淋巴结中ilc3的一小部分中表达。研究人员随后对两组小鼠进行基因改造:一组在胸腺中缺乏Aire,另一组在淋巴结中的ilc3中缺乏Aire。第一组患者产生了自身免疫,但成功地击退了念珠菌。相比之下,ILC3s中缺乏Aire的第二组小鼠没有自身免疫,但无法产生大量念珠菌特异性TH17岁的年代。因此,它们未能有效地消除念珠菌感染。换句话说,如果没有air表达ilc3,对抗假丝酵母菌所需的特化T细胞就不会产生足够数量。
“我们发现Aire有一个全新的作用,它在淋巴结中发挥作用——打开一种机制,增加对抗念珠菌的T细胞的数量,”dobekovsky解释道。
这些发现为未来的研究开辟了新的方向,可能有助于开发治疗严重念珠菌病的新疗法,也可能有助于治疗其他真菌感染。例如,新发现的机制可能有助于产生大量对抗念珠菌的T细胞用于细胞治疗。如果有一天科学家们能识别air - ilc3促进T细胞增殖的信号,这些信号本身就可能为新疗法提供基础。
进一步探索