早在17年前就能发现阿尔茨海默症
阿尔茨海默氏症是一种失智症,在最初的临床症状出现之前,有15到20年的无症状病程。利用波鸿开发的免疫红外传感器,一个研究小组能够在最初的临床症状出现前17年就在血液中识别阿尔茨海默氏症的迹象。传感器检测蛋白质生物标志物淀粉样蛋白- β的错误折叠。随着疾病的发展,这种错误的折叠会在大脑中造成特殊的沉积,即所谓的斑块。
“我们的目标是确定老年痴呆症在后期阶段的风险简单的血液测试甚至在有毒斑块在大脑中形成之前,为了确保治疗可以及时启动,”Ruhr-Universität波鸿蛋白质诊断中心(PRODI)的创始主任克劳斯·格沃特教授说。他的团队与位于海德堡(DKFZ)的德国癌症研究中心(German Cancer Research Center, DKFZ)由Hermann Brenner教授领导的团队合作进行了这项研究。
该团队在杂志上发表了用免疫红外传感器获得的结果阿尔茨海默症和痴呆2022年7月19日。本研究得到了a比较研究该研究于2022年3月2日发表在同一期刊上,研究人员在其中使用了互补单分子阵列(SIMOA)技术。
早期发现无症状的阿尔茨海默病高危人群
研究人员分析了血浆在萨尔进行的埃斯特研究的参与者中寻找潜在的阿尔茨海默氏症生物标志物。这些血液样本是在2000年至2002年间采集的,然后被冷冻起来。当时,测试参与者的年龄在50到75岁之间,尚未被诊断出患有阿尔茨海默氏症疾病.在目前的研究中,选取了68名在17年的随访中被诊断为阿尔茨海默氏症的参与者,并与240名未被诊断为阿尔茨海默氏症的对照组进行了比较。由克劳斯·格沃特和赫尔曼·布伦纳领导的研究小组旨在找出在研究开始时是否已经在血液样本中发现了阿尔茨海默症的迹象。
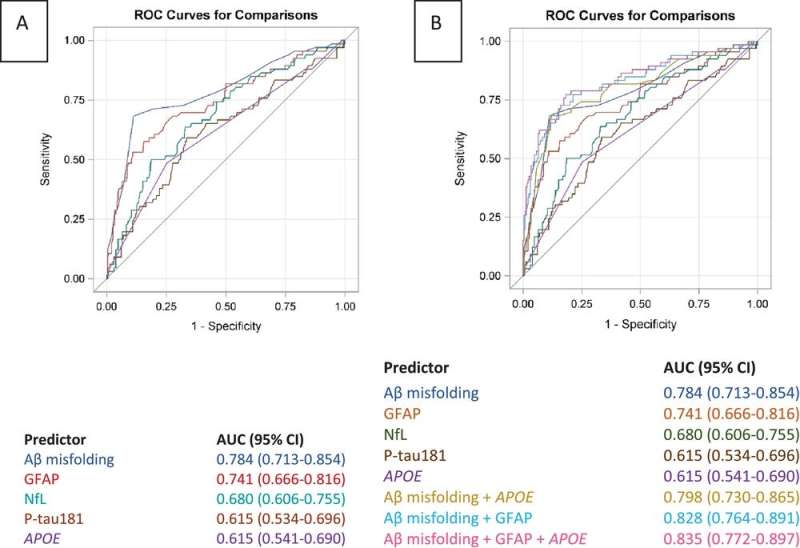
免疫红外传感器能够识别68测试对象他们后来患上了阿尔茨海默氏症,测试准确度很高。为了进行比较,研究人员检查了其他生物标志物与补充的、高灵敏度的SIMOA技术,特别是P-tau181生物标志物,目前在各种研究中被认为是有前途的生物标志物候选人。
克劳斯·格沃特说:“然而,与临床阶段不同的是,这个标记不适用于阿尔茨海默病的早期无症状阶段。”“令人惊讶的是,我们发现,神经胶质纤维蛋白(GFAP)的浓度可以在临床阶段前17年提示疾病,尽管它比免疫红外传感器要精确得多。”尽管如此,通过结合β淀粉样蛋白错误折叠和GFAP浓度,研究人员能够进一步提高无症状阶段检测的准确性。
初创公司的目标是将免疫红外传感器推向市场成熟
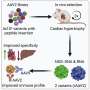
波鸿大学的研究人员希望早期诊断基于β淀粉样蛋白错误折叠的研究,可以帮助在阿尔茨海默病的早期阶段应用药物,使它们有明显更好的效果——例如,最近在美国获得批准的药物AduhelmKlaus Gerwert说:“我们计划使用错误折叠试验来建立一种老年人的筛查方法,并确定他们患阿尔茨海默氏症的风险。”
“我们新成立的初创公司betaSENSE的愿景是,在疾病发生不可逆转的损害之前,在没有症状的阶段停止这种疾病。”虽然该传感器仍处于开发阶段,但该发明已经在世界范围内获得了专利。BetaSENSE的目标是将免疫红外传感器推向市场,并获得批准作为诊断设备,以便在临床实验室中使用。
阿兹海默症药物的临床试验经常失败
药物Aduhelm于2021年春在美国获得FDA批准,已被证明可以清除大脑中的淀粉样- β斑块。然而,此前的研究表明,它对记忆丧失和方向感障碍等临床症状的影响很小。因此,欧洲药品管理局于2021年冬决定不批准该药物在欧洲销售。
“到目前为止,临床试验针对阿尔茨海默症的药物已经失败了十几个,显然是因为试验中使用的既定斑块测试没有及时标记出疾病,”Gerwert说。“似乎一旦斑块沉积,它们就会对大脑造成不可逆的损伤。”在迄今为止使用的测试中,斑块要么通过复杂而昂贵的PET扫描技术在大脑中直接检测到,要么通过ELISA或质谱技术在侵入性获得的脑脊液中利用蛋白质生物标志物浓度以一种不太复杂的方式间接检测。与已有的斑块诊断相比,免疫-红外传感器显示淀粉样蛋白- β的早期错误折叠,这导致了后来的斑块沉积。
Gerwert说:“然而,关于这种错误折叠是阿尔茨海默病的原因还是仅仅是伴随因素,仍有争议。”“对于治疗方法,这个问题是至关重要的,但它与诊断无关。这种错误折叠表明了阿尔茨海默病的发病。”
“治疗干预的确切时间在未来将变得更加重要,”Léon Beyer说,他是Klaus Gerwert团队的第一作者和博士生。“未来药物试验的成功将取决于研究参与者被正确地定性,并在研究开始时尚未显示出不可逆的损伤。”
帕金森症和渐冻症的生物标志物
错误折叠蛋白在许多神经退行性疾病中起着核心作用,如帕金森病、亨廷顿舞蹈病和肌萎缩性侧索硬化症(ALS)。正如研究人员所展示的,免疫红外传感器原则上也可以用于检测其他错误折叠的蛋白质,如TDP-43,这是肌萎缩性侧索硬化症的特征。他们不测量特定蛋白质的浓度,而是使用疾病特异性抗体检测其错误折叠。
Gerwert说:“最重要的是,这种平台技术使我们能够在神经退行性疾病的早期阶段进行基于生物标志物的鉴别诊断,目前应用的基于症状的诊断非常困难,而且容易出错。”
进一步探索
Hannah Stocker等人,血浆生物标志物p - tau181、胶质纤维酸性蛋白和神经丝光与中期和长期临床阿尔茨海默病风险的关系:来自一个随访超过17年的前瞻性队列的结果,阿尔茨海默症和痴呆(2022)。DOI: 10.1002 / alz.12614