干预阻止骨质流失

人体内的骨重塑涉及到成骨细胞(制造骨骼的细胞)和破骨细胞(破坏骨骼的细胞)之间的平衡。骨质疏松症、关节炎和牙周炎等疾病都涉及骨质流失,并与过度的破骨细胞活性有关。
在杂志上发表的一篇新论文中美国国家科学院院刊宾夕法尼亚大学(University of Pennsylvania)的研究人员及其同事对破骨细胞的调节提出了新的见解,有可能揭示导致疾病的失衡。这项研究发现,IFT80蛋白在控制破骨细胞数量方面起着关键作用。研究小组发现,缺乏IFT80的小鼠的破骨细胞数量比预期的要多,随后出现了严重的骨质减少。
“当你想到转化到临床时,我们认为这一发现非常重要,”宾夕法尼亚大学牙科医学院副教授、该研究的资深作者杨淑英(Sheri)说。“随着我们开始了解IFT80的机制和基因功能,我们可能会将其视为潜在的治疗靶点。例如,引入这种蛋白质的基于DNA或mrna的疗法可以帮助治疗某些疾病骨疾病。”
杨和同事在早期的一项研究后开始对IFT80感兴趣自然细胞生物学.它揭示了IFT,或鞭毛内蛋白,在T细胞蛋白运输中发挥作用。这些蛋白质是杨的实验室的研究重点,这一发现引起了她的兴趣,因为T细胞和破骨细胞都来源于此造血干细胞血细胞的前体。IFTs通过将蛋白质从纤毛的底部运输到顶端,然后再运输回来,帮助构建纤毛,纤毛是一种从细胞延伸出来的触角状感觉器官。在之前的工作中,Yang和其他人已经证明了IFTs在调节成骨细胞和软骨细胞(维持软骨的细胞)中起着关键作用间充质干细胞它们制造并维持骨骼、软骨和其他组织类型。
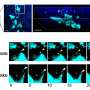
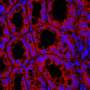
为了探索IFT80在破骨细胞中的作用,Yang的团队开发了一种敲除小鼠系,该敲除小鼠系缺乏破骨细胞前体中的蛋白质。值得注意的是,他们发现这些动物的骨容量明显低于正常小鼠,而它们的破骨细胞数量几乎增加了一倍。“这是一个巨大的变化,”杨说。
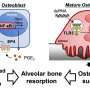
研究人员发现,IFT80可以防止破骨细胞前体引起骨吸收细胞并抑制破骨细胞成熟。
进一步实验表明,IFT80与破骨细胞中小调控蛋白泛素调控的蛋白降解途径中的Cbl-b蛋白相互作用。Yang的团队发现IFT80可以阻止Cbl-b的分解,而Cbl-b通常会降解另一种叫做TRAF6的蛋白质。TRAF6通常促进破骨细胞的产生,因此通过降解TRAF6, IFT80抑制破骨细胞分化。
在TRAF6的下游,研究小组还发现了IFT80抑制a信号通路由RANKL和RANK蛋白质控制。
为了验证IFT80是干预骨质丢失疾病的潜在靶点,研究人员在通常经历过度活跃的破骨细胞引起的骨质丢失的小鼠模型中过表达IFT80。这样做有效地抑制了RANK/RANKL的激活,降低了破骨细胞的产生,并增加了小鼠的骨容量。
这项研究首次将IFT80与破骨细胞的作用联系起来,并发现IFT80控制着a蛋白质在破骨细胞分化过程中起负调节作用。Yang说,这些特征使其成为潜在治疗干预的有价值的靶点。
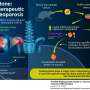
“现在人们对身体如何促进健康很感兴趣破骨细胞差异化,”她说。“很多疾病都与过度骨质流失有关——骨质疏松症、牙周炎、类风湿性关节炎甚至是骨折,都迫切需要找到解决方法骨质流失并恢复骨骼重塑的平衡。”
进一步探索
Francesca Finetti等人,TCR/CD3复合物向免疫突触的极化循环需要膜内转运,自然细胞生物学(2009)。DOI: 10.1038 / ncb1977