研究人员在透明细胞肾细胞癌中鉴定剪接变异生物标志物
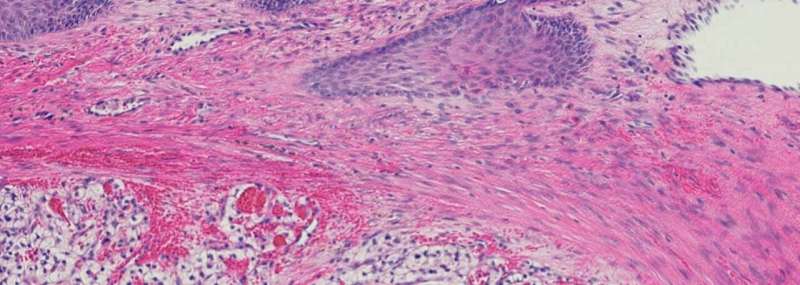
肾癌仅占美国所有癌症的4%;然而,自1975年以来,其发病率增加了一倍多,其中最常见的类型是透明细胞肾细胞癌。虽然由于新的治疗方案,患者的预后一直在改善,但患者的5年生存率为50%至69%,转移性疾病患者的5年生存率甚至更低。
科学家们正试图提高他们对透明细胞肾细胞癌发展的理解,以开发新的靶向治疗方法。一项新的研究发表在欧洲泌尿学莫菲特癌症中心的研究人员确定了这种疾病类型的生物标志物,并开发了一种工具,根据其生物标志物的表达来指示哪些患者具有不良预后的高风险。
透明细胞肾细胞癌是一种复杂的疾病,由于不同类型的基因突变而发展,包括遗传的改变和零星发展的改变。尽管有了这些知识,但这些突变都无法用于开发有效的治疗方法。为了更好地了解导致透明细胞肾细胞癌发展的关键分子过程,莫菲特的研究人员开始研究替代信使RNA (mRNA)剪接变体,以确定它们是否在这种疾病中发生改变,以及这些变体是否可以用作患者预后的生物标志物。
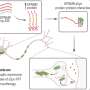
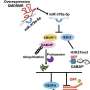
MRNA是将DNA转化为蛋白质过程中的关键中间分子。DNA在细胞核中被转化为信使rna。然后mRNA被用作模板,形成控制所有细胞和蛋白质生理过程;然而,在mRNA转化为蛋白质之前,RNA分子被拼接成不同的产物。这将启用单基因编码多种不同的蛋白质。替代拼接是一个自然的过程,但是癌症细胞可以劫持过程,创造剪接变异,有助于癌症的发展和进展。
Moffitt的研究人员使用了一种新的筛选过程,从癌细胞系数据开始,然后用透明细胞肾细胞癌患者的数据进行确认,以确定患者体内富集的剪接变异。他们确定了透明细胞肾细胞癌患者中发生改变的16个关键剪接变异,其中几个与疾病生物学和预后相关。研究人员还确定了几种剪接变异与改变的DNA修饰模式有关。
研究人员利用这些信息,基于五种剪接变体的组合表达水平创建了一种生存风险工具。RNASET2和FGD1的表达与不良预后相关,而PDZD2、COBLL1和PTPN14的表达与较好的预后相关。该工具能够根据总体生存和癌症特异性生存的低、中、高风险对患者进行分层。研究人员进一步分析了透明细胞肾细胞癌肿瘤样本中的蛋白质表达模式,发现在高危患者组中,几种负责基因剪接的蛋白质的表达和蛋白质修饰模式发生了改变。
“这些结果表明,改变剪接变异可能在透明细胞肾细胞的发育中发挥重要作用癌并代表患者预后的生物标志物,”研究作者、泌尿生殖肿瘤科助理成员布兰登·曼利博士解释道。“未来的研究需要阐明异常剪接变异的机制作用,预测对全身治疗的反应,以及作为疾病检测、复发或转移的生物标志物的应用。”
“发现了肾癌-特异性剪接变异体可能促进基于血液的液体活检检测的发展,以更好地管理疾病患者。我们正在测试这些RNA剪接变异是否也能在透明细胞患者的血液中检测到肾细胞癌.如果成功,我们将开发一种高度敏感的基于血液的方法来早期诊断这种疾病。这种非侵入性方法也可用于监测疾病进展,甚至预测治疗反应,”研究作者、泌尿生殖肿瘤科高级成员王亮博士说。
进一步探索