新的化学技术导致实验室中针对高风险白血病的更好的靶向治疗
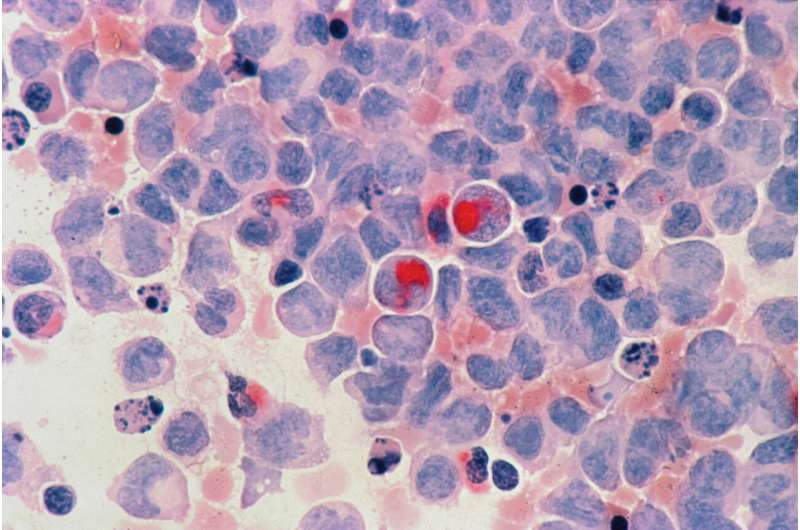
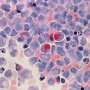
对于患有高危血癌t细胞急性淋巴细胞白血病(T-ALL)的儿童,急需更有效的治疗方法。圣裘德儿童研究医院的科学家利用最新的化学技术,即蛋白质水解靶向嵌合体(PROTAC),为这些患者开发了一种药物。研究结果发表在今天的科学转化医学.
之前的研究由St. Jude药剂学、药学科学和肿瘤学系的共同通讯作者Jun J. Yang博士领导,揭示了蛋白质LCK是44%的T-ALL儿童的重要药物靶点。工作,发表在自然癌症在2021年,证明了使用常见化疗药物达沙替尼治疗靶向LCK的可行性。不幸的是,像达沙替尼这样的小分子抑制剂有两个重要的弱点:它们通常只能暂时阻断靶标癌症细胞变异以规避药物的特殊作用。
“设计蛋白质的小分子抑制剂就像用钥匙把锁卡住一样,”杨说。“当它保持完全正确时,它的工作效果很好,但如果药物脱落,蛋白质将恢复其正常功能。PROTAC的方法是不同的。你没有阻止蛋白质目标,而是把它炸毁了,这样它就不存在了,永远不会回来了。”
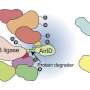
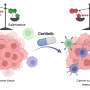
PROTACs:一种不同的靶向治疗方法
而不是阻塞靶蛋白, protac诱导目标降解,从而消除它。它们通过一种靶向机制使蛋白质(在这种情况下是LCK)接近E3泛素连接酶,然后标记它被细胞处理不需要的蛋白质的自然机制破坏。
共同通讯作者Zoran Rankovic博士,圣犹达化学生物学和治疗学系,使用一种新的E3连接酶导向基序,称为苯戊二酰亚胺,开发了圣犹达LCK-PROTAC SJ11646。该基序被证明优于PROTAC设计中常用的其他e3导向分子。研究人员此前发表了苯戊二酰亚胺的开发《应用化学》.
T-ALL的新疗法
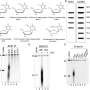
Yang, Rankovic和他们的同事表明SJ11646在消除LCK蛋白和杀死LCK激活的T-ALL方面非常有效。药代动力学和药动力学分析发现,与达沙替尼相比,SJ11646在患者来源的T-ALL异种移植模型中,LCK信号抑制的持续时间延长了630%。这种改善转化为白血病小鼠模型的延长生存期。
该研究为lck靶向PROTAC方法作为T-ALL的一种可能治疗方法提供了临床前原理证明。研究人员现在也在数百种其他癌症模型中测试SJ11646。他们的工作为开发更多的基于降解的治疗方法提供了蓝图。
“定向蛋白质降解是一种新的化学生物学范式,对药物发现有很大的希望,”Rankovic说。“虽然它仍需要优化用于白血病治疗,但我们有一个强有力的临床前原理证明,证明这种方法的可行性。”
这项研究的共同第一作者是圣裘德大学的胡建忠和杰米·雅鲁谢维奇。其他作者有宾夕法尼亚大学的David Teachey;以及杜国庆、西口吉赛尔、吉村聪、约翰·帕内塔、李振华、闵杰基、杨磊、迪夫亚巴拉希·切皮亚拉、玛丽莎·艾克斯、诺埃米·雷耶斯、布兰登·斯玛特和圣裘德的贝清汉。
进一步探索