研究发现新的痴呆风险基因通过新的检测方法

一项由加州大学洛杉矶分校领导的新研究发现了阿尔茨海默症和一种罕见的相关大脑疾病进行性核上性麻痹(PSP)的多个新的风险基因,该研究使用了一系列新的测试方法,允许在单一实验中对基因变异进行大规模筛选。
这项研究发表在今天的杂志上科学他还提出了一个经过修订的新模型,该模型显示了常见的遗传变异是如何通过扰乱基因组中的特定转录程序而提高患病风险的,尽管它们单独对疾病的影响非常小。
通常,研究人员依赖于全基因组关联研究(GWAS),在该研究中,他们调查了一大群人的基因组,以确定增加患病风险的基因变异。这是通过检测与疾病相关的染色体标记或基因座来实现的。每个基因座平均有数十个——有时是数百或数千个——共同遗传的遗传标记,因此与疾病有关,这使得识别哪些是真正引起疾病的功能性变异变得困难。
确定因果变异及其影响的基因是现代遗传学和生物医学的主要挑战。本研究为解决这一问题提供了一个有效的路线图。
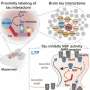
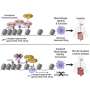
对于这项研究,作者进行了已知的第一个高通量测试来研究神经退行性疾病。作者进行了大规模的平行报告分析(MPRAs),同时测试了与阿尔茨海默氏症相关的25个位点和与PSP相关的9个位点的5706个基因变异,PSP是一种比阿尔茨海默氏症罕见得多的神经疾病,但有着类似的病理。
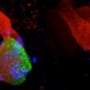
从那次测试中,作者以很高的信心确定了320个功能性基因变异。为了验证结果,他们对42个高置信度变异的多种细胞类型进行了CRISPR筛选。
“我们结合了多项进展,使人们能够进行高通量生物学,而不是一次做一个实验,而是以一种池的形式并行地进行数千个实验。这项研究的通讯作者、加州大学洛杉矶分校的戈登和弗吉尼亚麦克唐纳人类遗传学、神经病学和精神病学特约教授丹·格什温德博士说:“这使我们能够从与一种疾病相关的数千种遗传变异转移到确定哪些是功能性的,哪些是它们影响的基因。”
他们的数据为阿尔茨海默症的几个新的风险基因提供了证据,包括C4A、PVRL2和odp1,以及PSP的其他新的风险基因(PLEKHM1和KANSL1)。作者还能够验证几个之前确定的风险位点。Geschwind说,下一步将是研究新发现的风险基因如何在细胞和模型系统中相互作用。
Geschwind说,这项研究证明了高通量测试可以为进一步研究提供“非常有效”的路线图,但他强调,这些方法必须与更有针对性的实验相结合,就像在这项研究中一样。
他说:“这一成功并不意味着我们可以放弃在模型系统中研究个体基因的详细、仔细的实验。”“这只是提供了GWAS和理解疾病机制之间的关键一步。”
该研究的主要作者尤纳坦·库珀(Yonatan Cooper)说,研究人员采用的综合方法让他们对自己的发现更有信心,同时也突显了解释人类基因变异的固有挑战。
“我们相信,多种方法的整合对未来在研究和临床领域注释疾病相关变异的工作至关重要,”库珀说,他是医学博士/博士。加州大学洛杉矶分校大卫格芬医学院医学科学家培训项目的候选人。
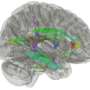
作者还能够在PSP中显示出至少一种机制,在这种机制中,与疾病相关的多个位点共同作用,破坏了一组核心转录因子,这些转录因子本质上是打开和关闭基因的,已知这些转录因子在特定的细胞类型中共同工作。Geschwind说,这说明了共性遗传变异在整个基因组中影响特定细胞类型的特定调节网络。他说,这一发现确定了新的潜在药物靶点,并表明针对基因网络而不是针对一个基因可能是一种有效的方法。
Geschwind说:“我们正在进入一个治疗的新阶段——考虑靶向网络开始变得合理。”
进一步探索