研究人员探索通过固定细胞来治疗癌症
未来晚期癌症的治疗方法可能是将癌细胞固定在适当的位置,防止它们在全身扩散。加州大学戴维斯分校和华盛顿大学的研究人员进行的一项新研究显示了抗体如何加强细胞之间的联系。该研究发表于8月3日美国国家科学院院刊.
华盛顿大学(University of Washington)和西雅图儿童研究所(Seattle Children’s Research Institute)的巴里·冈比纳(Barry Gumbiner)教授开发的单克隆抗体19A11能与e -钙粘蛋白(E-cadherin)结合,e -钙粘蛋白是一种帮助细胞结合在一起的蛋白质,尤其是在皮肤、肠道和其他器官的上皮层中。钙粘蛋白和其他粘附分子对维持血管结构和预防癌症转移以及在炎症和相关疾病如克罗恩病和炎症性肠病中发挥作用。
研究人员此前发现,用19A11治疗可以防止肺扩散癌症小鼠细胞。
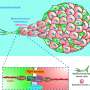
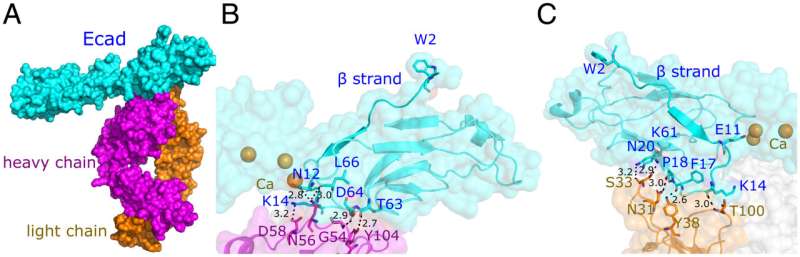
生物物理学研究生谢斌,生物医学工程系Sanjeevi Sivasankar教授,以及加州大学戴维斯分校和西雅图分校的同事们,对19A11如何与e -钙粘蛋白结合进行了详细的研究。利用x射线晶体学,他们发现抗体与e -钙粘蛋白结合的位置靠近它与另一个e -钙粘蛋白分子的连接位置。通过模拟和原子力显微镜的结合,他们发现19A11有两个绑定模式,其中一种模式增加了E-cadherin的粘结强度。这种增加的粘附性来自于分子之间形成的一种称为盐桥的化学链接。
通过更好地了解这种抗体如何增加细胞之间的粘性,研究人员希望找到方法,按照相同的思路设计更有效的治疗方法。
本文的其他作者是:加州大学戴维斯分校的安德鲁·普里斯特;西雅图儿童研究所和华盛顿大学的Allison Maker;David Dranow, Jenny Phan和Thomas Edwards,西雅图感染性疾病结构基因组学中心和UCB制药公司;Bart Staker和Peter Myler,西雅图传染病结构基因组学中心和西雅图儿童研究所。
进一步探索