白血病漏洞发现导致药物敏感性
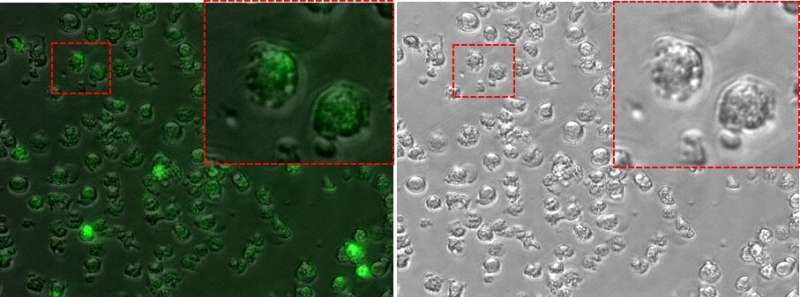
所有人类肿瘤来自各种组织分享一系列属性定义,包括防止细胞死亡的能力。相反,健康的器官诱导细胞程序性死亡或凋亡平衡它们的大小和消除受损的细胞。有一个特定的和生理细胞死亡叫ferroptosis发生诱导的氧化脂肪由铁含量。
今天,在《华尔街日报》发表的一篇文章生物氧化还原领域的期刊引用自由基和癌症,群Esteller博士,主任约瑟卡雷拉斯白血病研究所(IJC) ICREA大学研究教授和主席遗传学巴塞罗那,和由卢卡斯Pontel博士表明,表观遗传变化防止iron-associated编程细胞死亡在白血病和试验药物治疗的新目标。
“白血病细胞避免死亡,因为他们有两个浮点数,生物分子称为谷胱甘肽的代谢和FSP1基因作为抵御这个铁和氧化引起的死亡,“Esteller博士的评论。“学习这些代谢途径我们意识到在急性淋巴细胞白血病(ALL)的活动FSP1基因epigenetically丢失,所以这些细胞程序性死亡的悬崖的边缘。我们只需要给他们一个促进和管理我们的谷胱甘肽通路的抑制剂,如L-BSO RSL3,迅速诱导这些恶性淋巴细胞的死亡。换句话说,这种类型的白血病生活边缘的宽容ferroptosis当你与药物消除他们的最后的救命稻草,这些转化细胞死亡。这个弱点急性淋巴细胞白血病因此可以探索在精度和个性化的治疗这种疾病,但它也可能发生在其他癌症。很少有临床试验与谷胱甘肽抑制剂在肿瘤,但也许这种类型的工作将引起兴趣的研究和开发这些有前途的实验人员,”研究人员说。
Pontel博士说:“通过研究t和b患者的数据,我们发现,FSP1是表观遗传控制。因此,通过确定FSP1表观遗传状态的病人,我们可以预期治疗的成功基于药物诱导ferroptosis。”
进一步探索