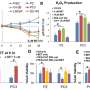
Pralsetinib对RET基因融合患者实现了组织不可知的好处

根据德克萨斯大学MD Anderson癌症中心的研究人员领导的国际I/II期ARROW试验的结果,高选择性RET抑制剂pralsetinib在RET融合阳性癌症患者中具有良好的耐受性,并表现出强大、持久的反应,无论肿瘤类型。
研究结果发表在今天的自然医学, 23个国家的总有效率为57%,疾病控制率为83%病人患有多种癌症。这些发现建立在之前在ret - modified中报道的积极结果的基础上非小细胞肺癌(NSCLC)和甲状腺癌,提示靶向治疗可能为RET融合患者提供组织不可知的好处。
“我们已经在临床下一代测序方面取得了爆炸性进展,这使我们能够了解多种肿瘤类型中共享的生物标记物,而这项研究对于确定RET融合是否适用于各种癌症类型是很重要的,”研究癌症治疗学副教授、通讯作者Vivek Subbiah医学博士说。“我们观察了与肿瘤类型、先前治疗或基因融合伙伴无关的反应。这些数据证实了RET是一个对RET抑制敏感的组织不可知靶点。”
当含有RET基因的染色体片段破裂并与另一条染色体重新结合时,就会发生RET融合,从而产生一种融合蛋白,为癌症提供燃料。RET改变在甲状腺髓样癌、甲状腺乳头状癌和非小细胞肺癌中最常见,但在许多其他组织类型中很少发生。
基于该试验的早期结果,美国食品和药物管理局(fda)于2020年9月批准普alsetinib用于治疗RET融合阳性NCLSCs,并于2020年12月批准普alsetinib用于治疗晚期RET改变甲状腺癌。
为了确定该疗法是否在非小细胞肺癌和甲状腺癌以外提供了益处,这项开放标签的单臂研究还招募了各种RET融合阳性实体瘤患者。该队列中的常见癌症包括胰腺癌、胆管癌、神经内分泌肿瘤和肉瘤。
该研究招募了29名患有12种不同癌症类型的患者。其中,23例患者能够根据数据截止日期和预先指定的评价标准进行疗效评价。这些患者的中位年龄为53岁;14例(61%)为女性。种族统计数据中65%是白人,30%是亚裔,4%是黑人。大多数患者有转移性疾病(87%),并接受过癌症治疗(87%)。
其中,3例(13%)患者确诊为完全缓解,10例(43%)患者确诊为部分缓解。中位缓解时间为11.7个月中位无进展生存期是7.4个月,而中位总生存期13.6个月。
25例(86%)患者出现了治疗相关的副作用,20例(69%)患者出现了3级或以上的不良事件。最常见的副作用是肝酶天冬氨酸转氨酶和丙氨酸转氨酶水平升高,白细胞水平降低(中性粒细胞减少)。共有17名患者(59%)出现短期剂量中断,13名患者(45%)因副作用出现永久性剂量减少。
Subbiah说:“尽管除了肺癌和甲状腺癌,RET融合非常罕见,但这些患者需要有效的治疗。”“这些发现证明了RET抑制剂有潜力使不同肿瘤类型的患者受益,并显示了精准医疗的力量,可以将患者匹配到正确的类型靶向治疗基于他们的独特特征癌症."
展望未来,Subbiah和他的同事将专注于RET抑制剂耐药机制,以进一步改善RET改变患者的预后。他的团队已经开始识别耐药性途径,并致力于开发新的治疗方法。