团队获得了对遗传和分子机制的见解,使个人容易患阿尔茨海默氏病
西奈山研究人员已经对人类小胶质细胞的遗传和分子机制(存在于大脑中的免疫细胞)实现了前所未有的理解,该细胞可以为它们如何促进阿尔茨海默氏病的发展和发展(AD)提供宝贵的见解。该团队的发现发表在自然遗传学。
研究人员使用活检或尸检收获的新鲜人脑组织,研究人员确定了21种候选风险基因,并突出显示了SPI1,是小胶质细胞和AD风险的潜在关键调节剂。
高级作家Panos Panos Roussos,精神病学教授,遗传学和基因组科学教授,高级作家Panos Roussos说:“我们的研究是遗传危险因素的最大人类新鲜组织小胶质细胞分析,可能使某人患上阿尔茨海默氏病。”在西奈山的伊坎医学院和疾病神经基因组学中心主任。“通过更好地理解分子和遗传机制参与小胶质细胞功能,我们处于更好的位置,可以揭示控制功能并有助于AD的调节景观。反过来,这种知识可能为目前没有有效治疗的疾病的新型治疗干预铺平道路。”
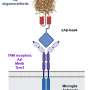
小胶质细胞主要负责大脑中的免疫反应,也对神经元的发展和维持至关重要。虽然先前的研究,包括西奈山(Mount Sinai),已经确定小胶质细胞在阿尔茨海默氏病的遗传风险和发展中起着关键作用,但对发生这种情况的表观遗传力学知之甚少。因为小胶质细胞在隔离人脑,大多数先前的研究都使用了基于动物或细胞系的模型,这些模型并不反映大脑中小胶质细胞功能的真实复杂性。另一个挑战是将AD遗传风险变化与特定的分子功能有关风险因素经常在基因组的非编码部分(过去称为“垃圾DNA”)中发现,这很难研究。
西奈山团队的解决方案是通过四个脑生物学家之间的合作,三个在西奈山和拉什大学医学中心/拉什阿尔茨海默氏病中心之间的合作,从活检或尸检中获取新鲜的脑组织。“使用来自这些来源的150个样本,我们能够分离出高质量的小胶质细胞,通过反映健康和神经退行性患者中的小胶质细胞的整个调节成分,,这为遗传调节提供了前所未有的见解。”。
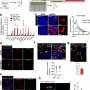
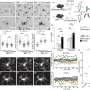
该过程 - 与表观遗传相结合,基因表达, 和遗传信息从AD和健康老年患者的样本中,允许研究人员全面描述小胶质细胞功能如何在人类中遗传调节。作为其统计分析的一部分,他们扩大了先前全基因组关联研究的发现,以将鉴定出的AD预先培养的遗传变异与特定的DNA调节序列和基因联系起来,其失调直接有助于疾病的发展。他们进一步描述了整个细胞的调节机制是鉴定小胶质活性特定方面涉及的遗传区域的一种方式。
从他们的研究中出现了有关科学家已经知道的SPI1基因的新知识,它是调节与AD基因相关的其他转录因子和基因网络的主要小胶质细胞转录因子。该团队正在产生的数据对于破译其他神经退行性疾病背后的分子和遗传谜团也可能很重要,其中小胶质细胞在其中发挥作用,包括帕金森氏病,多发性硬化症和肌萎缩性侧面硬化症。
鲁索斯博士承认,他的团队仍在全面了解鉴定的基因如何促进阿尔茨海默氏病的发展和发展,以及如何使用新的治疗剂。不过,他的实验室的实验室的单细胞分析结果极大地鼓舞了他小胶质细胞使用高度复杂的仪器,这些乐器正在发现不同类型的不同类型之间的独特相互作用免疫细胞在里面脑及其与神经退行性疾病有关的外围。Roussos博士报告说:“我们通过单细胞数据看到了非常令人兴奋的结果,这使我们越来越接近理解诸如阿尔茨海默氏症之类的遗传性疾病的遗传驱动变异和细胞特异性相互作用。”
进一步探索