发现治疗常见遗传性心脏疾病肥厚性心肌病的新方法
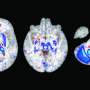
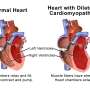
耶鲁大学Qyang和Campbell实验室的Muhammad Riaz博士、Jinkyu Park博士和Lorenzo Sewanan博士领导的研究提供了一种机制来识别与遗传性心脏疾病肥厚性心肌病(HCM)相关的异常,在这种情况下,左心室壁变得异常厚且经常僵硬。研究结果发表在该杂志上循环.
家族性HCM患者猝死风险增加,心脏衰竭,以及心律失常。HCM是最常见的遗传性心脏病,每500人中就有一人患病。这种疾病被认为是由调节心肌收缩的突变引起的,这种突变损害了心脏泵血的能力。然而,人们对这种疾病背后的机制知之甚少。
在这项多模型研究中,研究人员使用干细胞方法来了解驱动遗传HCM的机制。技术,诱导多能干细胞(iPSCs),可以加速对疾病遗传原因的洞察,并利用患者自身开发新的治疗方法细胞.
“这是一次令人谦卑的经历,患者的疾病表型教会了研究人员基本的基础知识,为创新的新疗法奠定了基础。此外,我们的研究已经建立了一个很好的模型,可以帮助耶鲁大学医学院和耶鲁大学纽黑文医院的许多医生利用患者自己的iPSCs和工程组织来揭示疾病进展的机制,”医学(心脏病学)和病理学副教授qyibing Qyang博士说。
“我们想了解疾病的机制,并找到一种新的治疗策略,”Park说。
这个概念起源于一位18个月大的家族性HCM患者。通过与Daniel Jacoby医学博士合作,心血管医学兼职副教授和HCM专家,他提供了医疗保健对于这名患者,Park和团队使用干细胞技术解决了一个基本问题,即HCM背后的疾病机制。他们收集了10毫升患者的血液,并将干细胞因子引入血细胞中,以产生可自我再生的iPSCs。通过应用心脏知识,他们诱导诱导多能干细胞进入患者自己的心肌细胞(心脏细胞)心脏疾病研究。“我们发现了一个普遍的机制来解释疾病进展朴槿惠说。
接下来,他们设计了与年轻患者早发性疾病相似的心脏组织。该疾病在18个月大时表现严重,这表明该疾病始于胎儿/新生儿阶段。
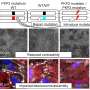
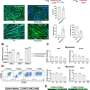
研究的下一阶段是重建一个3D模型,用于模拟疾病的进展,包括机械性能比如肌肉的收缩和力的产生,以了解如果突变存在,有多少力会受损。这项研究是由耶鲁大学生物医学工程系的Stuart Campbell博士和Sewanan博士合作完成的。再加上计算模型为肌肉收缩,作者开发了强大的系统,使他们能够在三维水平上检查组织的生物力学特性。
最后,研究团队利用先进的基因编辑技术,对这些突变进行了修改。他们发现,在突变被纠正后,疾病就逆转了。这些关于肌肉蛋白突变的见解可能会为HCM和其他疾病带来新的治疗方法。突变之间的相互作用也可能表明,在缺血性心脏病等其他疾病中存在相同的生物力学机制。
Riaz说:“我们可以将这些发现应用于与高血压、糖尿病或衰老相关的心脏疾病。”
Riaz补充说:“一个根本的挑战是我们需要从患者的家庭中产生iPSCs。”利用这项技术,Park能够从HCM患者的细胞中重建原代细胞,这个过程需要一个多月的时间。Riaz和Park使用干细胞来确定由肌肉瘤引起的病理组织重塑的重要作用肥厚性心肌病突变。
Riaz说:“我们希望我们的发现能在科学界得到复制。”“这是一个从床到实验研究的例子,科学家从诊所提取材料,在实验室进行实验,然后发现治疗患者的新方法。”
作者还指出,RNA测序可以作为在分子水平上表征疾病的指南。科学家们可以通过检查组织的生物力学特性来鉴定出更有针对性的药物。他们说:“我们现在可以筛选多种药物,看看这些药物中是否有任何一种能够挽救这种表型。”
进一步探索