3 d瀑样模型识别潜在的毁灭性的小儿肾脏疾病治疗的目标
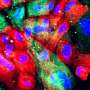
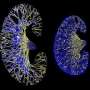
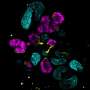
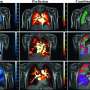
![CDH1<sup>+</sup> distal nephron dilates in <i>PKHD1<sup>−/−</sup></i> kidney organoids cultured under flow.(<b>A</b>) Schematic of kidney organoid-on-a-chip (flow) culture and static culture. (<b>B</b>) Diagram of differentiation days and culture conditions for flow and static culture. (<b>C</b>) Representative phase-contrast images of <i>PKHD1<sup>−/−</sup></i> and <i>PKHD1<sup>+/−</sup></i> organoids cultured under flow on days 16 to 18, days 21 to 25, and day 32 of differentiation. Red arrows highlight dilated tubules. Scale bars, 100 μm (top). Representative phase-contrast images of <i>PKHD1<sup>−/−</sup></i> and <i>PKHD1<sup>+/−</sup></i> organoids cultured under flow on day 35 of differentiation. White arrows highlight dilated tubules. Dashed white lines highlight normal tubules. Scale bar, 50 μm (bottom). (<b>D</b>) Immunocytochemistry with sample clearing for proximal tubule (LTL and CFTR) and distal tubule (CDH1) in <i>PKHD1<sup>−/−</sup></i> organoids with and without flow on day 35. Scale bar, 100 μm. (<b>E</b>) Bright-field images of patient-derived ARPKD organoids with and without forskolin treatment in 3D culture on day 66. Scale bar, 250 μm (top). Immunocytochemistry for proximal tubule (LTL), distal tubule (CDH1), and podocyte (PODXL) in <i>PKHD1<sup>−/−</sup></i> organoids with and without forskolin treatment on day 35. Scale bar, 100 μm (bottom). (<b>F</b>) Tubular diameters in nephron segments [proximal tubule (LTL) and distal tubule (CDH1)] in <i>PKHD1<sup>−/−</sup></i> organoids with and without flow (left) and with and without forskolin treatment (right). Values represent means ± SD. **<i>P</i> < 0.01, ****<i>P</i> < 0.0001. Credit: <i>Science Advances</i> (2022). DOI: 10.1126/sciadv.abq0866 3 d瀑样模型识别潜在的毁灭性的小儿肾脏疾病治疗的目标](https://scx1.b-cdn.net/csz/news/800a/2022/3d-organoid-models-ide.jpg)
Organoids-lab生长细胞或组织类似organs-serve作为疾病的新工具建模,但研究人员往往很难复制生物物理身体内的器官运作条件。
特别是建模需要刺激的细胞微环境的人类疾病。
来自马萨诸塞州综合医院的一个研究小组,布莱根妇女医院,Wyss研究所和他的同事们最近曼联与organ-on-a——瀑样芯片技术复制的独特疾病过程潜在的常染色体隐性多囊肾疾病(APRKD)。
在最近的一项研究科学的进步团队,是由肯冢,医学博士,博士和Ryuji Morizane,医学博士,博士报告使用新的建模系统来识别两个潜在APRKD疗法,目前没有fda批准的治疗。
APRKD是一种障碍,其特征是在肾脏囊肿的形成,扩大器官,导致肾脏功能的逐步丧失。有报道在婴儿死亡率高达30%。对于那些患者生存,41%需要肾移植11岁。
PKHD1疾病的致病基因,但是以前曾试图模型的疾病转基因小鼠模型已经成功。研究人员已经能够在实验室里培养细胞突变PKHD1。然而,这种疾病在静态三维建模瀑样不工作,因为它是由突变引起的表面的细胞刺激的尿流。
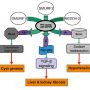
克服这一挑战,团队使用了一个3 d打印机创建一个灌注芯片,模型在肾细胞的微环境,并允许液体流瀑样。这样团队确定了两个mechanosensing分子(安全系数和RAC1)疾病的潜在治疗靶点。
他们还阐明关于ARPKD疾病机制的两个重要问题:
- 分子的安全系数可能是一个重要的种专一性囊肿形成的制止,这也解释了为什么小鼠模型无法有效地复制疾病
- 为什么PKHD1基因的突变导致囊肿形成吗
团队还测试了两种fda批准的药物(R-Naproxen和R-Ketorolact)抑制RAC-1和一个试验性新药,抑制”丛书(t - 5224),这都显示在这些模型有治疗效果。
临床试验将需要调查这些ARPKD患者的治疗。瀑样建模系统的成功复制疾病还可能帮助研究人员发现更多的潜在的治疗目标。
“在这项研究中,我们表明,肾脏瀑样芯片平台上提供了一个生理ARPKD相关模型,允许mechanosensing信号的识别作为cystogenesis的关键因素,”Morizane说,一名调查员在神经学部门质量一般,哈佛医学院助理教授。
“在我们的研究结果验证,fda认可的非甾体抗炎药,抑制RAC1抑制剂以及临床试验的安全系数显示在我们的模型中有治疗效果。我们的观察突出organoid-on-a-chip的巨大潜力模型来阐明复杂的疾病的治疗机制检测和发现。”
进一步探索