唤醒休眠细胞抗癌的功效
小分子靶向治疗的出现,十年前,彻底改变了治疗转移性黑色素瘤,肿瘤携带突变应对这些疗法。然而,尽管一个了不起的最初反应,可以看到在大多数患者中,他们中的大多数将经历复发甚至在壮观的最初反应。这些复发是由于休眠细胞,持续对治疗。
日内瓦大学的一个团队(UNIGE)和日内瓦大学医院(拥抱)已经表明,这些细胞under-express一种叫做户珥的蛋白质。通过解密机制的表达式,通过瞄准一个不足酶抑制剂,这个团队已经成功地减少了治疗抵抗的黑素瘤细胞。这些结果发表在生物化学和生物物理研究通信,开辟新的治疗途径转移性黑色素瘤固体和其他类型的癌症。
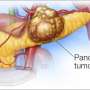
黑色素瘤是一种最危险的皮肤癌。可能非常激进,它的发展从黑色素细胞,细胞负责皮肤色素沉着。最初的肿瘤可以在去除表面与预后良好,也可以越来越成为转移,转移到身体的其他器官。
过去十年,由于出现所谓的小分子靶向therapies-drugs抑制肿瘤内的确切机制对抗一半携带基因的转移性黑色素瘤的签名让他们对这些药物敏感,可以有效治疗,有时甚至被根除。”然而,尽管这种壮观的最初反应,80%的病人会复发,而且这些复发往往会出现在相同的最初影响网站,“解释Rastine Merat,美国医学研究员UNIGE医学院和头部Onco-dermatology单元的拥抱。
蛋白调节细胞分裂
这种现象被称为“自适应抵抗”:确定癌症细胞适应药物用于对抗他们,导致疾病的复兴。这种情况即使转移,因此细胞,使这些tumors-seem完全消失了。“这是解释为持久性,治疗后,小残留的所谓的“休眠”恶性肿瘤细胞传统的放射学工具无法检测,“说Rastine Merat。“这些细胞的特殊性,除了是无形的,是它们繁殖缓慢。这一特点可以帮助细胞逃避治疗,甚至在最初的治疗。”
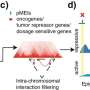
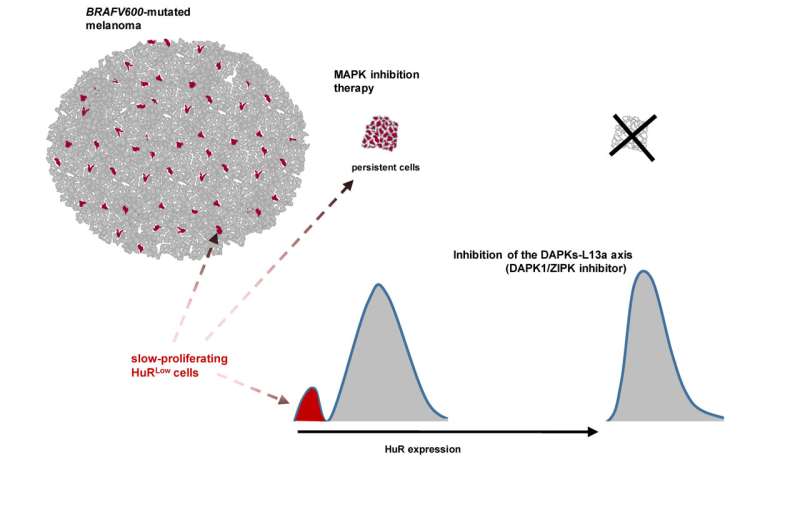
此前进行的研究表明,在slow-proliferating细胞,一种蛋白质,这种蛋白质等调节许多基因控制的表达细胞分裂——户珥蛋白质不够表达。这是在与快速增殖的细胞蛋白质高度表达。在2019年发表的一项研究工作,Rastine Merat和他的团队建立了这种蛋白质的表达不足之间的联系和黑色素瘤细胞抵抗的能力靶向治疗。在最近的研究中,他们发现了一种特定的机制参与不足表达“休眠”这种蛋白质的细胞可以有针对性的药物。
抑制酶,以防止复发
”细胞,信使rna蛋白质生产中发挥核心作用。少数细胞,户珥不够表达,我们发现被困户珥的信使rna由其他蛋白质。这是至少一个机制,使户珥表达不足。”By using a化合物在这个机制,抑制两个kinases-enzymes-involved UNIGE团队设法防止户珥表达不足,减少所有黑色素瘤细胞的能力抵抗治疗。
“伟大的困难工作的开展这项工作是这种类型的细胞,这是很难发现和分析,因为他们人数不多,户珥蛋白质的表达不足的状态是动态的和可逆的在任何时间任何细胞;即。,在任何时候相同的细胞可以开始增殖并翻转这种蛋白的高表达状态,”研究员解释道。要做到这一点,“我们矛盾的是在黑色素瘤细胞中这种蛋白质。这使得我们可以更容易的机制在起作用。”This discovery opens new perspectives in the treatment of melanoma, but not only. "Melanoma is a model cancer: if we understand it, we can understand many other types of solid cancers," explains Rastine Merat.
研究员和他的团队,“下一步将是鼓励制药行业优化确定激酶的抑制剂,——提高其稳定性和bioavailability-which是制药制药公司现在知道如何在一个系统的方式,至少对于这种类型的目标,”总结Rastine Merat。
进一步探索