为了将儿童癌症从地图上抹去,科学家们必须绘制出它的基因组图谱
科学家们已经绘制了最常见的儿童癌症——急性淋巴细胞白血病(ALL)的基因突变路线图。圣犹大儿童研究医院的这项研究首次提供了all所有亚型基因组学的全面观点。这项工作为医生和科学家了解疾病发展和改善治疗结果提供了基础指导。这项研究发表在今天的自然遗传学.
“在这项研究中,我们能够全面地定义在儿童ALL中发现的反复改变的基因的数量和类型,”圣犹大病理学系M.B.B.S博士、共同通信作者Charles Mullighan说。“由于这项研究的规模,我们可以识别出许多在白血病或癌症中根本没有报道过的新关联基因,并表明它们属于几种新的细胞通路。”
创建路线图以理解ALL
由于圣犹大等机构的科学家和临床医生的工作,大多数患有ALL的儿童将存活下来。然而,这些患者中的一小部分对治疗反应不佳。科学家们认为,这些患者癌症基因的差异可以预测治疗反应。例如,圣犹大研究小组发现,在通常被认为风险较低的白血病中,单一的特定基因重排与复发风险显著增加有关。
如果研究人员了解基因差异对癌症结果的影响,那么在未来,医生可以在开始治疗前对患者的癌症进行测序。这将使医生能够根据患者的基因和对不同抗癌疗法的反应可能性,对患者进行个性化治疗。
但在将个性化疗法引入临床之前,科学家需要在不同疾病亚型中绘制驱动白血病发展的不同突变。
费城儿童医院的共同通讯作者Stephen P. Hunger医学博士说:“这项研究的发现清楚地定义了ALL的许多不同基因亚型。”“这些基因亚型中有几个以前是未知的,我们还发现了导致ALL发展的常见的次生和三级突变。我们能够确定精准医疗治疗的新途径,从而潜在地提高治愈率,减少治疗的短期和长期副作用。”
这项研究的独特之处在于,它包括了2574例小儿ALL患者样本,这是迄今为止发表的最大的此类队列。相比之下,早期的研究通常只研究了数百个样本,甚至更少。圣犹大的研究人员与儿童肿瘤小组合作,在十多年的时间里收集样本。
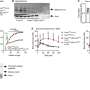
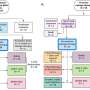
对样本进行全基因组、全外显子组或转录组组合测序。研究人员通过比较这些序列来寻找突变的模式。这些模式可以作为了解癌症如何发展以及对治疗的反应的路线图。
“这项研究证明了数据的力量,”共同通讯作者、圣犹大计算生物学系主任张景辉博士说。“如果你没有足够数量的患者样本,你就缺乏统计能力来发现患病率低的司机。一旦我们有了动力,我们就发现了一个参与ALL开发的新驱动群体。”
她说:“新的驱动因素包括一种蛋白质修饰,这非常令人兴奋,因为我们过去从未预料到这组蛋白质会参与白血病的疾病启动。”
一系列有趣的结果
由圣犹大大学的Sam Brady博士和Kathryn Roberts博士领导的研究人员寻找新的驱动基因突变。平均而言,儿童癌症样本有四种导致ALL发展的突变。
总的来说,该小组发现了376个显著突变的潜在驱动基因癌症发展。其中70个基因从未与ALL相关。一些意想不到的潜在驱动突变存在于相关基因中细胞过程如泛素化、sumo化或非编码顺式调控区域。
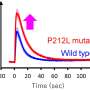
研究人员还发现,ALL亚型的突变存在差异,这可能会影响临床护理.例如,其中两组涉及特定的基因重排,这与cepa /FLT3或NFATC4基因表达不同。这一观察结果可能具有临床意义,因为新的FLT3抑制剂正在进行临床试验,这表明cepa /FLT3 ALL亚型可能对这种疗法敏感,但其他亚组可能不敏感。
所有癌症的发展都始于染色体的“大爆炸”
研究人员的工作揭示了许多ALL病例中突变事件的顺序,对治疗有潜在的影响。在双倍体b细胞ALL中,癌症细胞至少比正常多5条染色体(人类多46条)。在ALL的发展过程中,染色体增加和其他突变的相对时间是一个长期存在的问题。了解这一过程将为白血病的发展提供重要的见解。
研究人员通过对突变序列和染色体增益数据的计算建模,追踪导致高二倍体ALL的事件顺序。这表明,在大多数双二倍体B-ALL病例中,染色体增益似乎发生得很早,而且是一次性的,这是染色体的“大爆炸”。然后,癌前细胞增加更多突变部分原因是紫外线引起的DNA损伤。这一发现表明紫外线损伤会导致急性淋巴细胞性白血病,这是一个以前有争议的观点。
进一步探索
圣犹大影响力门户:platform.stjude。云/数据/寇…ccession = sjc - ds - 1009