根据一项新研究,人类细胞中的抗病毒酶加速了COVID-19的突变
研究人员发现了首个实验证据,解释了为什么COVID-19病毒会如此迅速地产生delta和omicron等变异。
该研究结果发表在9月13日的杂志上科学报告这项技术可以帮助科学家预测新的冠状病毒毒株的出现,甚至可能在这些毒株到来之前生产出疫苗。
多种COVID-19病毒变体的出现相对较快,这让研究人员感到困惑,因为大多数冠状病毒不会如此迅速地变异和进化。这是因为他们有一个内置的“校对”机制来防止突变当它们在我们的细胞中生长和繁殖时,它们会自我复制。
但南加州大学的科学家们发现了COVID-19病毒绕过校对的策略:它劫持了内部的酶人类细胞它们通常会防御病毒感染他们利用这些酶改变其基因组并制造变异。
首席研究员陈晓江(音译)是南加州大学多恩西夫文理学院的生物科学和化学教授,他说,这些发现有助于防止新变种引起的感染激增,对遏制大流行至关重要。
陈说:“新毒株的传染性会越来越强,并逃避现有疫苗的保护。”“预测新的变异并提前准备有效的疫苗可以在新变异传播之前阻止它们。”
防守是最好的进攻
Chen和南加州大学的团队在实验室中用冠状病毒感染了人类细胞,然后研究了病毒在细胞内复制自身时基因组的变化。
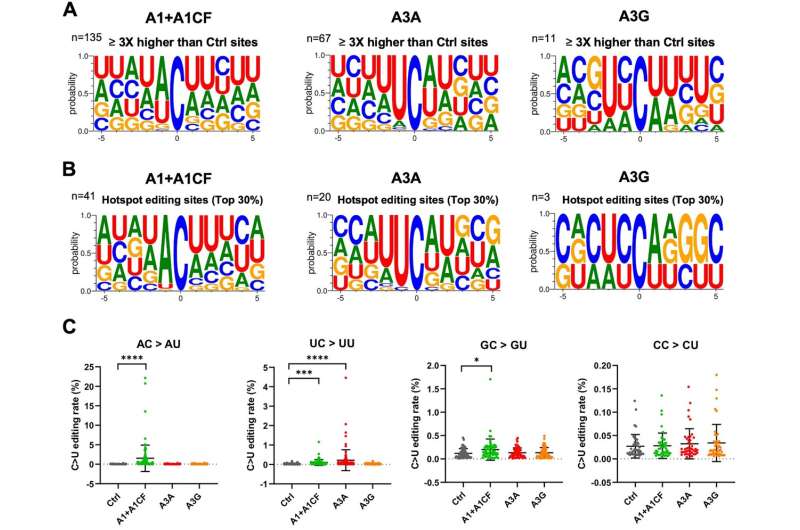
病毒的遗传密码序列由DNA的近亲RNA组成,用四个字母来识别组成核苷酸:A、C、G、u。在分析过程中,Chen和团队注意到一个有趣的模式:病毒复制自身时产生的许多突变都是由代码中的一个特定核苷酸改变为另一个核苷酸引起的——字母“C”变成了“u”。
c到u的高频率突变指向了一组细胞经常用来防御病毒的酶。这种酶被称为APOBEC,它将病毒基因组中的c转化为Us,目的是引起致命的突变。
但Chen和他的团队发现,对于在人类细胞中生长的COVID-19病毒来说,从c到u的突变不仅不致命,而且还为病毒提供了一种比预期更快地突变、进化和发展新毒株的途径,从而使病毒受益。
陈说:“我们提供了第一个实验证据,证明我们自己的酶可以帮助COVID-19病毒快速变异。”“不知怎的,病毒学会了扭转这些宿主APOBEC酶的进化和适应性。”
扭转局面
幸运的是,对于希望克服COVID-19的研究人员来说,每一次进攻都有弱点。在这种情况下,APOBEC酶产生的突变不是随机的——它们在基因序列中的特定位置将C转化为U,在这些位置U或a刚好在C之前(如UC或AC)。
有了这一见解,科学家们可以寻找COVID-19病毒基因组中的每一个UC和AC,并使用强大的计算和实验方法,预测和测试如果其中任何一个变成u会发生什么。这可以帮助他们预测可能出现的新COVID-19变体,并建议如何更新疫苗,以防止任何可能传播的新变体。
Chen和他的团队的目标就是做到这一点,研究APOBEC酶引起的c到u突变可能对COVID-19病毒的生命周期及其传播和致病能力产生什么潜在影响。随着时间的推移,这些信息可以帮助科学家生产新的药物和疫苗,以击败耐药和逃避疫苗的COVID-19病毒菌株。
进一步探索