研究人员确定了多囊肾疾病的基因治疗靶点
德克萨斯大学西南研究人员报告称,通过删除microRNAs的结合位点来阻断PKD1和PKD2基因表达的抑制,可以阻碍常染色体显性多囊肾病(ADPKD)模型肾囊肿的形成和生长。该研究结果发表在自然通讯,提出了一种有可能阻止或治愈ADPKD的基因治疗策略。
“25年多来,我们已经知道ADPKD是由PKD1或PKD2基因突变引起的。然而,目前还没有针对这些根本原因的治疗策略,”UTSW肾内科副教授Vishal Patel医学博士说,他也是该论文的通讯作者。
ADPKD是最常见的人类遗传疾病之一,也是肾衰竭最常见的遗传原因,全世界约有1250万人受到影响。ADPKD是一种遗传性疾病,患者通常遗传一个PKD1(或PKD2)突变副本和一个正常副本。
该疾病的特征是经常形成许多小的充满液体的囊,称为肾囊肿,这被认为是PKD1或PKD2水平低于临界阈值时形成的。当基因的正常拷贝不能产生足够的多囊素-1/多囊素-2蛋白时,就会发生这种情况。
蛋白质由基因的信使核糖核酸(mRNA)产生(或翻译)。在mRNA链的一端是一个编码区域,它有助于保护mRNA不被降解,但也可以控制蛋白质的制造量。microRNAs与mRNA编码的这一区域的结合可以阻断翻译,导致蛋白质的产生减少。
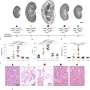
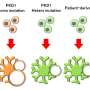
PKD1包含一个结合位点miR-17是一种在ADPKD模型中高表达和活跃的microRNA。因此,帕特尔博士和他的同事们询问,阻断miR-17与PKD1的结合是否可以防止肾囊肿的形成。
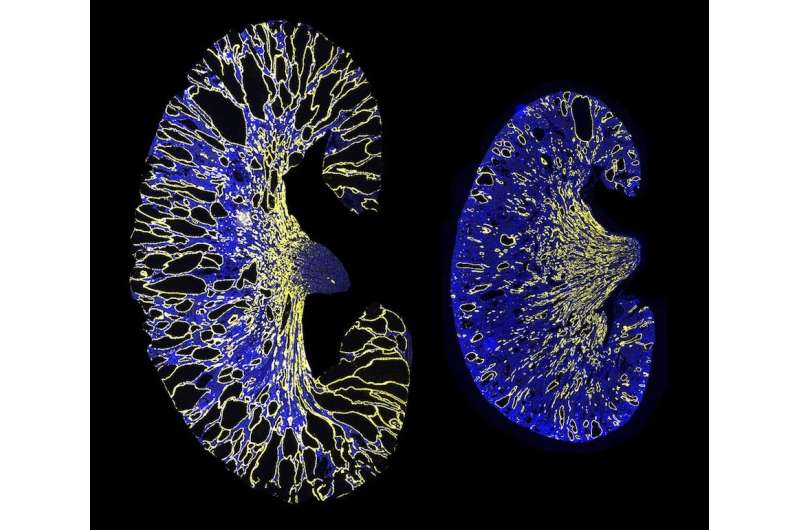
研究人员从PKD1 mRNA中删除了miR-17结合位点细胞培养ADPKD小鼠模型。他们的结果表明,删除结合位点增加了mRNA链的稳定性,提高了多囊素-1水平,并减少了肾囊肿的生长。此外,该小组发现,在囊肿形成后,用抗miR-17药物阻断miR-17与PKD1 mRNA的结合也减少了囊肿的生长,这表明这种相互作用可能是一种有希望的靶点多囊肾病(PKD)治疗。
“在许多遗传条件下,致病基因的一个副本发生了突变,但另一个副本仍然正常。我们利用剩余正常拷贝的方法可能适用于PKD以外的许多其他疾病,”Patel博士说。
进一步探索