研究揭示了血细胞中的癌前“克隆生长”
一项由威尔康奈尔医学院、纽约长老会医院、纽约基因组中心、哈佛医学院和丹娜-法伯癌症研究所的研究人员共同领导的研究表明,血液干细胞中常见的自发突变可能会通过改变干细胞的基因活性程序和它们产生的血细胞混合来促进这些疾病的发生。这种突变与血癌和心血管疾病的高风险有关。
这种被称为DNMT3A R882的血液干细胞突变会导致循环血细胞大量繁殖,或称为“克隆生长”,这些循环血细胞也含有这种突变。一般来说,随着年龄的增长,这种突变生长变得越来越常见,并被认为代表了非常早期的恶性肿瘤前期阶段癌症发展。
然而,分子细节它们是如何产生的还很难确定,因为突变细胞的外观和功能与正常细胞大致相同。在研究中,它出现在自然遗传学,研究人员克服了这一挑战,阐明了DNMT3A中R882突变的影响,DNMT3A是血细胞中最常见的突变基因。
“这些发现帮助我们了解这些突变细胞是如何超越正常细胞生长的,并为未来可能针对这些细胞的干预措施铺平了道路,以防止癌症和其他克隆生长相关的情况,”纽约长老会/威尔康奈尔医学中心的肿瘤学家、该研究的资深作者丹·兰道博士说。
这项研究是兰道博士的实验室与哈佛医学院(Harvard Medical School)医学教授、达纳法伯癌症研究所(Dana Farber Cancer Institute)的艾琳·戈布里亚尔博士(Irene Ghobrial)的实验室合作进行的。戈布里亚尔博士的团队提供了血液干细胞从多发性骨髓瘤缓解期患者的骨髓中,他们发现,在这些患者中,血细胞克隆生长是相对常见的。
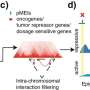
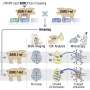
兰道博士的团队评估了来自患者的6000多个细胞,使用“单细胞多组学”技术检测DNMT3A R882突变,并进行绘制基因活性以及DNA上被称为甲基化的化学标记,即关闭附近基因的编程标记。通过这种方法,他们前所未有地详细记录了含有突变的血液干细胞与正常干细胞的区别。
例如,研究人员发现,突变干细胞产生成熟血细胞的比例向红色倾斜血细胞以及产生凝血血小板的细胞——这为糖尿病的高风险提供了潜在的理论依据心血管病在血液中有克隆增生的病人身上。
DNMT3A基因通常编码一种被称为甲基转移酶的酶,这种酶有助于在DNA上放置甲基化。研究人员发现,这种突变对正常甲基化的破坏导致整个基因组缺乏这些“关闭开关”,并导致关键基因的异常激活。后者包括炎症驱动基因和癌症相关生长基因——所有这些都与突变细胞的生长和生存优势相一致,并与它们发展为癌症的更高风险相一致。
“我们希望通过发现这样的分子特征,我们将能够针对这些克隆生长,并在仍然健康的人中预防癌症的发展,”该研究的共同第一作者Anna Nam博士说,她是病理学和实验室医学系的病理学和实验室医学助理教授,威尔康奈尔医学的迈耶癌症中心的成员,纽约长老会/威尔康奈尔医学中心的病理学家。
研究人员计划对其他突变导致的克隆生长进行进一步研究。他们还在开发多组学技术,以提高这些研究的速度和规模。
“我们很快就能同时对更多的细胞进行研究,让我们对发生的事情有一个更完整的了解,”联合第一作者、三所学院的医学博士内维尔·杜萨伊(Neville Dusaj)说。朗道实验室的项目学生。
进一步探索