揭示甲状腺癌对lenvatinib-a产生耐药性的机制之一
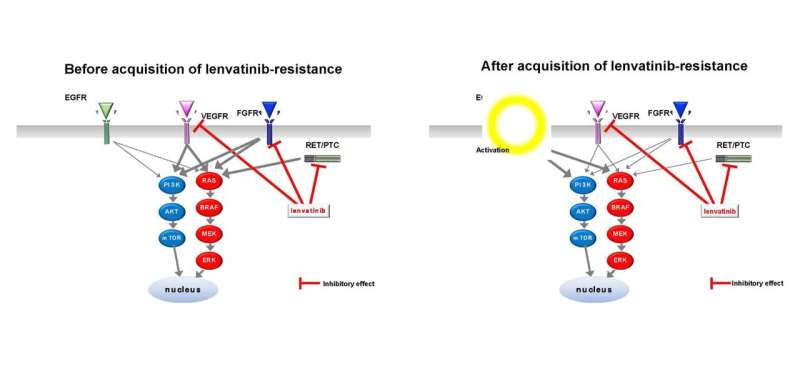
多靶点酪氨酸激酶抑制剂(MKI) lenvatinib被广泛用于治疗晚期和转移性甲状腺癌。然而,甲状腺癌细胞对lenvatinib产生耐药性的分子机制仍然知之甚少。在这项研究中,我们首次证明了表皮生长因子受体(EGFR)介导的信号通路的激活与甲状腺癌细胞的lenvatinib耐药有关。
虽然甲状腺癌是最常见的内分泌恶性肿瘤,目前有效的药物很少。Lenvatinib是一种MKI,已广泛用于晚期和转移性甲状腺癌的治疗。不幸的是,一些癌症从治疗一开始就对lenvatinib耐药或对治疗产生耐药。因此,必须阐明lenvatinib耐药的机制,以制定更好、更有效的治疗晚期甲状腺癌的策略。利用培养的甲状腺癌细胞系,来自日本信州大学医学院外科乳房和内分泌外科的研究人员在分子水平上研究了这些机制。
研究人员从两个亲本甲状腺癌细胞系(TPC-1和FRO)中建立了lenvatinib耐药亚线(即TPC-1/LR和FRO/LR),并发现在TPC-1/LR细胞中EGFR、细胞外信号调节激酶(ERK)和Akt的磷酸化被促进。此外,通过给药激活EGFR通路表皮生长因子(EGF)对TPC-1和FRO产生耐药前诱导lenvatinib敏感性降低。相反,EGFR抑制剂拉帕替尼与lenvatinib同时给药TPC-1/LR细胞,其中EGFR磷酸化上调,增强了lenvatinib的生长抑制作用。
接下来,在用lenvatinib耐药TPC-1/LR细胞移植的裸鼠异种移植物模型中,lenvatinib联合拉帕替尼治疗被抑制肿瘤的生长比lenvatinib单药治疗效果更显著。
此外,当lenvatinib对信号转导途径在6个甲状腺癌细胞系中进行分析,在所有细胞系中都观察到EGFR磷酸化的增强,无论细胞系起源的组织学类型或驱动基因突变的存在。然而,下游信号分子(如ERK和Akt)的磷酸化水平在不同细胞系之间存在差异。
为了验证拉帕替尼联合lenvatinib抑制EGFR是否增强了lenvatinib的生长抑制作用,我们同时对这6种细胞系进行了两种药物的治疗。因此,在最初对lenvatinib不太敏感的三种细胞系中观察到生长抑制的协同增强。
Lenvatinib的抗肿瘤作用主要通过有效抑制血管内皮生长因子受体1-3 (VEGFR1-3)、成纤维细胞生长因子受体1-4 (FGFR1-4)的活性和转染期间基因重排(RET)发挥作用。本研究结果表明,EGFR,一种酪氨酸激酶受体(TKR),不是lenvatinib的靶分子,在lenvatinib给药期间被激活,并可能使甲状腺癌细胞对lenvatinib产生耐药性。这项研究表明,联合lenvatinib和EGFR抑制剂抑制EGFR通路可能是增加lenvatinib敏感性和克服甲状腺癌lenvatinib耐药的一种新的治疗策略。
甲状腺癌分为以下类型:起源于滤泡上皮细胞的分化型甲状腺癌、间变性甲状腺癌和起源于滤泡旁细胞的髓样癌。虽然间变性甲状腺癌仅占甲状腺癌的2%左右,但其预后极差。相反,大约90%的甲状腺癌是分化型甲状腺癌,包括乳头状癌和滤泡癌。分化型甲状腺癌的标准治疗是手术和放射性碘治疗,10年疾病特异性生存率为> 90%。然而,有些癌症对放射性碘治疗有耐药性,已经转移到远处器官的分化癌症的10年生存率< 50%。
驱动基因突变,如BRAF、RAS和RET/PTC突变,在甲状腺癌细胞中经常发现。然而,在甲状腺癌中观察到TKRs下游的丝裂原激活蛋白激酶信号通路的激活,如FGFR, VEGFR或血小板衍生生长因子受体(PDGFR),无论驱动基因突变是否存在。此外,MKIs已被用于治疗对放射性碘疗法难以治疗的分化型甲状腺癌。Lenvatinib是一种口服MKI,靶向VEGFR1-3, FGFR1-4, PDGFR和RET,已在全球广泛使用,因为它在放射性碘难治性分化甲状腺癌的III期研究中延长了无进展生存期。
然而,主要的临床挑战,如一些癌症从治疗开始就对lenvatinib耐药,以及在治疗过程中出现耐药,继续普遍存在。因此,为了克服lenvatinib耐药,有必要识别预测lenvatinib敏感性的生物标志物,并阐明甲状腺癌细胞获得lenvatinib耐药的分子机制。
- lenvatinib耐药细胞系的建立甲状腺癌细胞TPC-1 (RET/PTC突变)和FRO (BRAFV600E突变)在lenvatinib存在下延长培养时间;抗性系TPC-1/LR(抗性是亲本细胞的140倍)和FRO/LR(抗性是亲本细胞的5.3倍)被建立并用于研究。
- 细胞内信号通路变化的测定利用western blotting (WB)分析信号分子的蛋白表达和磷酸化,以确定lenvatinib耐药的获得改变细胞内信号转导的机制。
- 药敏分析采用水溶性四唑盐(WST-1)法分析了lenvatinib单独、EGF存在及联合拉帕替尼对甲状腺癌细胞株的生长抑制作用。
- 药物抗肿瘤作用的体内分析:将lenvatinib耐药TPC-1/LR细胞皮下植入裸鼠,建立荷瘤模型,分析lenvatinib单用及联合lapatinib的抗肿瘤作用。此外,收集肿瘤组织,进行WB和免疫组化。
传播效果及未来规划
Lenvatinib已广泛用于治疗放射性碘治疗耐药的晚期和转移性分化甲状腺癌。然而,一旦癌症对这种药物产生耐药性,就没有有效的治疗策略。这项研究的结果表明,lenvatinib和EGFR抑制剂的联合使用可以提高lenvatinib的疗效,并可能成为晚期甲状腺癌的一种新的治疗策略。
BRAF抑制剂和MEK抑制剂联合应用于BRAF V600E突变阳性间变性甲状腺癌的临床实践,通过联合多种分子靶向药物抑制生长关键信号通路的治疗策略已应用于其他几种恶性肿瘤的临床实践。本研究的结果有力地表明,多种分子靶向药物的联合将在未来治疗恶性肿瘤的策略中发挥重要作用。
该团队计划探索其他lenvatinib耐药机制与分子机制lenvatinib诱导EGFR激活甲状腺癌症细胞。
这项研究发表在癌症科学.