基因疗法能迅速改善先天性失明成人的夜视能力
宾夕法尼亚大学佩雷尔曼医学院的Scheie眼科研究所的研究人员称,患有遗传形式的儿童期起病性失明的成年人在接受实验性基因疗法的几天内,夜视能力有了惊人的恢复。
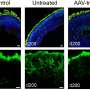
的病人他患有莱伯先天性黑蒙(LCA),这是一种由基因GUCY2D突变引起的先天性失明。研究人员的研究结果发表在该杂志上iScience根据临床试验方案,该公司将携带健康版本基因的DNA的AAV基因疗法注入每位患者一只眼睛的视网膜。在接受治疗的几天内,每位患者的眼睛都显示出由杆状光感受器细胞介导的视觉功能大幅增强。杆状细胞对光极其敏感,占了人类弱光视觉能力的大部分。
“这些令人兴奋的结果表明,光转导的基本分子机制在一些LCA病例中基本保持完整,因此即使在失明几十年之后也可以接受基因治疗,”该研究的主要作者Samuel G. Jacobson医学博士说,他是宾夕法尼亚大学的眼科学教授。
LCA是最常见的先天性失明疾病之一,大约每4万新生儿中就有1人患有此病。视力丧失的程度因人而异,但所有LCA患者从生命最初的几个月起就有严重的视力障碍。有二十多个基因其功能障碍可导致LCA。
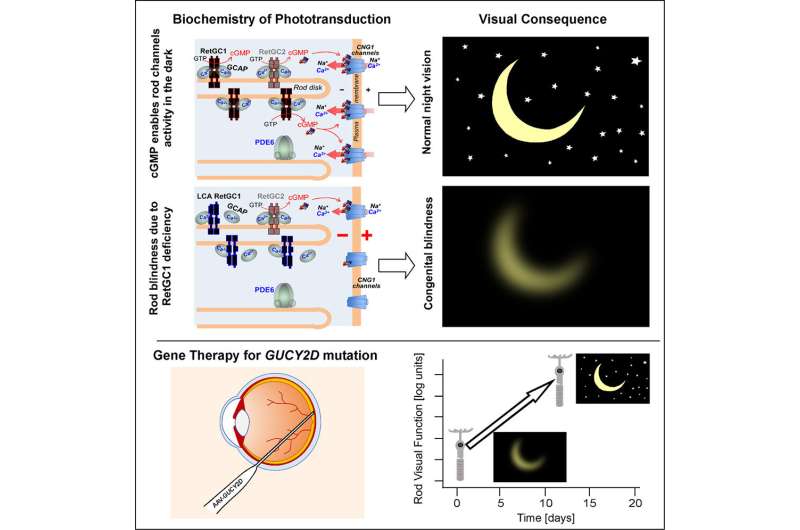
高达20%的LCA病例是由GUCY2D基因突变引起的,该基因编码视网膜光感受器细胞中“光转导级联”所需的关键蛋白质,“光转导级联”是将光转换为神经元信号的过程。先前的影像学研究表明,这种形式的LCA患者往往有相对保存的光感受器细胞,特别是在棒状细胞丰富的区域,提示棒状光转导可以再次工作,如果功能GUCY2D存在。去年报告的低剂量基因疗法的早期结果与这一想法一致。
研究人员对两名患者使用了高剂量的基因疗法,一名19岁的男性和一名32岁的女性,他们有特别严重的视杆视觉缺陷。在白天,患者的一些视觉功能虽然严重受损,但在晚上,他们实际上是失明的,对光的敏感度是正常人的1万到10万倍。
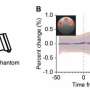
研究人员只对每个患者的一只眼睛进行了治疗,因此可以将治疗过的眼睛与未治疗过的眼睛进行比较,以衡量治疗效果。视网膜手术由Thomas Jefferson大学和Wills眼科医院的眼科教授Allen C. Ho医学博士完成。测试显示,在两名患者中,经过治疗的眼睛在弱光条件下对光敏感度提高了数千倍,基本上纠正了最初的视觉缺陷。研究人员总共使用了九种互补的方法来测量患者的光敏感度和功能性视力。这些测试包括在弱光条件下的房间导航技能测试和瞳孔对光线的不自觉反应测试。测试持续显示出基于视杆的低光视力的重大改善,患者也注意到他们日常生活的功能改善,例如“现在可以在黑暗中辨认物体和人。”
“同样令人惊讶的是,治疗后改善的速度很快。在8天内,两名患者已经显示出可衡量的疗效,”研究合著者、宾夕法尼亚大学眼科研究教授Artur V. Cideciyan博士说。
对研究人员来说,结果证实了GUCY2D基因治疗恢复基于杆的光感受器功能,并提示有更严重的杆性功能障碍的GUCY2D-LCA患者可能从该疗法中获益最大。实际的信息是,在筛选LCA候选人和在整个治疗试验中监测他们时,应该强调杆视觉测量。
研究人员说,这些发现还强调了一个值得注意的事实,即在一些患有严重先天性视力丧失的患者中,视网膜细胞网络起着调节作用愿景保持大体的存活和完整,只需要补充缺失的蛋白质就能开始工作,或多或少会立即开始工作。
进一步探索