研究人员开发了治疗三阴性乳腺癌的“金发女孩药物”
经过几十年的研究和之前的两次药物开发尝试,亚利桑那大学的一组研究人员正在研究一种针对一种特定类型乳腺癌的低毒性治疗方法,前景看好。
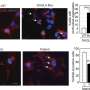
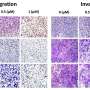
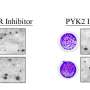
研究人员已经开发出一种似乎可以停止的药物化合物癌细胞的生长在所谓的三阴性乳腺癌.这种药物尚未在人体上进行试验,但已被证明可以消除小鼠体内的肿瘤,对正常健康细胞几乎没有影响,因此对患者可能无毒。
这种疗法是基于一种新发现的方式,一种叫做表皮生长因子受体即EGFR,会导致癌症。EGFR是一种长期研究的致癌基因,这种基因在特定情况下可以将细胞转化为肿瘤细胞。
研究人员的研究结果发表在该杂志上癌症基因治疗该团队正在努力获得美国食品和药物管理局(Food and Drug Administration)的批准,以便在人体上测试该化合物的第一阶段临床试验。
三阴性乳腺癌约占所有乳腺癌的10%到15%。根据美国癌症协会(American cancer Society)的说法,三阴性指的是癌细胞对其他三种类型的乳腺癌检测呈阴性,这些类型的乳腺癌是由过多的雌激素、孕酮或HER2蛋白引起的。三阴性乳腺癌在40岁以下黑人或BRCA1基因突变的女性中更为常见。根据美国国立卫生研究院(National Institutes for Health)的数据,大约一半的三阴性乳腺癌病例过度表达EGFR致癌基因。
亚利桑那大学的研究人员设计了一种化合物,可以阻止EGFR进入驱动癌症存活的细胞部分。这种化合物会关闭EGFR蛋白的功能,EGFR蛋白作用于癌细胞,而不是正常细胞。
通常情况下,药物在攻击时没有足够的针对性,所以它们会攻击其他健康细胞的部分,导致不必要的副作用。研究人员希望阻止这种情况的发生。
Joyce Schroeder说:“EGFR被认为是一种致癌基因已经有60年了,有很多药物都试图针对它,但它们都有局限性,不能使它们成为治疗乳腺癌的药物。”Joyce Schroeder与分子与细胞生物学系的博士后Benjamin Atwell共同撰写了这篇论文。
施罗德领导着该大学的分子和细胞生物学系,并领导着进行论文研究的实验室。她也是该大学BIO5研究所和癌症中心的成员。
她和她的团队发明的前两种药物技术可以杀死癌细胞,但它们存在问题。
在他们的第一次尝试中,研究人员瞄准了施罗德所说的EGFR蛋白质的“非结构化”部分,结果,该化合物不能持续和可靠地发挥作用。
第二次尝试的结果是,一种化合物过于宽泛,击中了蛋白质的一部分,这部分蛋白质也驱动健康细胞的正常活动,使药物具有毒性。
为了有效,施罗德和她的团队知道,他们必须开发一种化合物,可以进入癌细胞,并针对EGFR基因产生的蛋白质的准确部分,阻止癌症的扩散。他们第三次尝试成功了。
“这就像金发姑娘效应,”施罗德说。
她和她的团队知道,他们必须找到一种既不会影响正常细胞,又能在体内保持活性的解决方案。
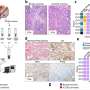
她说:“当我们在动物模型上测试这种药物时,我们得到了这个令人难以置信的结果,它实际上不仅阻止了肿瘤的生长,它还导致肿瘤退缩和消失,而且我们没有看到任何毒副作用。”“我们对此非常兴奋,因为它是肿瘤特异性的。”
分子和细胞生物学家理想地设计药物化学,就像设计一把钥匙来打开一个非常特殊的锁一样靶蛋白完全正确的方式,仅此而已。
施罗德说:“针对三阴性乳腺癌一直很困难,因为它没有这些明显的目标。”“人们很早就知道三阴性乳腺癌细胞会表达EGFR,但当已知的EGFR药物扔给它时,它没有反应。”
许多研究人员认为可能EGFR不应该是靶标,所以他们寻找新的靶标。另一方面,施罗德认为EGFR只是以一种研究人员尚未理解的方式在起作用。她和她的团队试图以一种新颖的方式瞄准它,并取得了成功。
下一步,除了人体试验,是测试药物抑制转移的能力癌症细胞扩散到身体的其他部位,施罗德说。
研究人员一直致力于保护知识产权并进一步与Tech Launch Arizona进行授权,Tech Launch Arizona是一个将大学创新商业化的大学办公室。
进一步探索