尽管有高血压却没有心脏损伤:检查磷酸二酯酶3A基因突变的影响
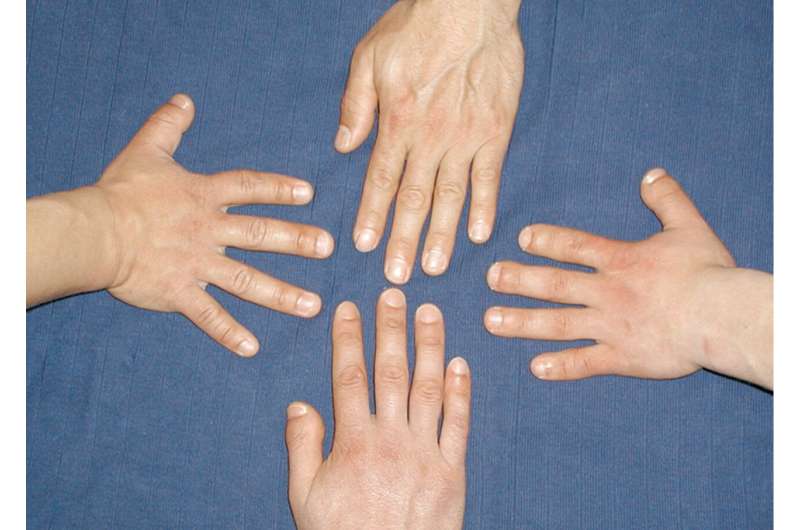
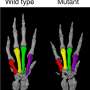
几十年来,柏林的科学家们一直在研究一种奇怪的遗传疾病,这种疾病会导致某些家庭的一半成员手指异常短,血压极高。如果不及时治疗,受影响的患者通常会在50岁时死于中风。
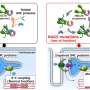
柏林Max Delbrück中心(MDC)的研究人员早在2015年就发现了这种疾病的原因,并在五年后通过动物模型证明了他们的假设:磷酸二酯酶3A基因(PDE3A)的突变导致其编码的酶过度活跃,影响骨骼生长,导致血管增生,从而导致血压升高。
对高血压相关损伤免疫
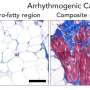
“高血压几乎总是导致心Max Delbrück中心锚定信号实验室负责人、德国心血管研究中心(DZHK)的科学家Enno Klußmann博士说。Klußmann解释说,由于它必须承受更高的压力,该器官试图加强左心室。“但最终,这会导致心肌增厚,即心脏肥厚,从而导致心力衰竭,大大降低其泵血能力。”
但对于手指变短和PDE3A基因突变的高血压患者来说,这种情况不会发生。Klußmann说:“由于目前部分但尚未完全了解的原因,他们的心脏似乎对通常由高血压引起的损害免疫。”
这项研究已经发表在杂志上循环,是Max Delbrück中心、Charité-Universitätsmedizin Berlin和DZHK的研究人员合作的结果。除了Klußmann,来自Max Delbrück中心的Norbert Hübner教授和Michael Bader教授是最终作者,还有来自实验和临床研究中心(ECRC)的Sylvia Bähring博士,该中心是Charité和Max Delbrück中心的联合机构。
与来自柏林、波虹、海德堡、卡塞尔、林堡、Lübeck、加拿大和新西兰的43名其他研究人员一起,该团队现在报告了他们关于基因突变的保护作用的发现——以及为什么这些结果可能改变未来心脏衰竭的治疗方式。该出版物有四位第一作者,其中三位在Max Delbrück中心进行研究,另一位在ECRC。
两种突变产生了相同的效果
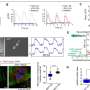
科学家们对…进行了测试人类患者患有高血压和短指畸形(HTNB)综合征,即高血压以及异常短的手指——以及大鼠模型和心肌细胞。这些细胞是从被称为诱导多能的特殊工程干细胞中培养出来的干细胞.在测试开始之前,研究人员改变了细胞和动物中的PDE3A基因,以模仿HTNB突变。
“在我们检查的患者中,我们发现了一种之前未知的PDE3A基因突变,”Bähring报道。“以前的研究一直表明,酶中的突变位于催化结构域之外,但我们现在发现了一个突变就在这个结构域的中心。”
令人惊讶的是,这两种突变具有相同的效果,它们使酶比平常更活跃。这种过度活跃加剧了细胞中一种重要信号分子cAMP(环磷酸腺苷)的降解,cAMP与心肌细胞的收缩有关。Bähring说:“这种基因修饰——不管其位置如何——可能导致两个或更多PDE3A分子聚集在一起,从而更有效地工作。”
蛋白质保持不变
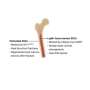
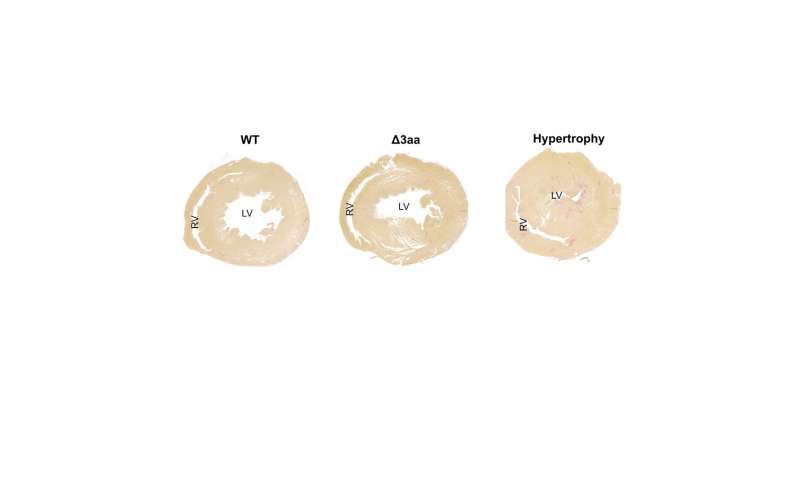
研究人员使用了一个大鼠模型——由Max Delbrück中心的迈克尔·巴德实验室用CRISPR-Cas9技术创建——试图更好地理解突变的影响。“我们用异丙肾上腺素治疗动物,这是一种所谓的β受体激动剂,”Klußmann说。这类药物有时用于终末期心力衰竭患者。已知异丙肾上腺素可诱发心肌肥厚。
“然而令人惊讶的是,这种情况发生在转基因大鼠身上,其方式与我们在野生型动物身上观察到的类似。与我们预期的相反,现有的高血压并没有加剧情况,”Klußmann报道。“他们的心脏明显不受异丙肾上腺素的影响。”
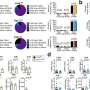
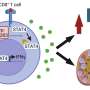
在进一步的实验中,研究小组调查了心肌细胞特定信号级联中的蛋白质是否因突变而发生了变化,如果是的话,是哪些蛋白质发生了变化。通过这一连串的化学反应,心脏对肾上腺素做出反应,在兴奋等情况下心跳加快。
肾上腺素激活细胞的β受体,使它们产生更多的cAMP。PDE3A和其他pde通过化学改变cAMP来阻止这一过程。“然而,我们发现突变型和野生型大鼠在蛋白质和RNA水平上几乎没有区别,”Klußmann说。
胞浆中的钙增多
PDE3A对cAMP的转化并不仅仅发生在心肌细胞的任何地方,而是发生在存储钙离子的管状膜系统附近。这些离子释放到细胞的细胞质中会引发肌肉收缩,从而使心脏跳动。收缩后,钙被蛋白质复合物泵回储存。这个过程也由PDE在本地进行规范。
Klußmann和他的团队假设,因为这些酶在钙泵周围的局部区域非常活跃,所以应该有更少的camp——这将抑制钙泵的活性。“在基因修饰的心肌细胞中,我们实际上发现钙离子在胞浆中停留的时间比平时更长,”Klußmann实验室的成员、该研究的四名第一作者之一Maria Ercu博士说。“这可以增加细胞的收缩力。”
激活而不是抑制
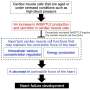
Klußmann解释说:“PDE3抑制剂目前用于急性心衰治疗,以提高cAMP水平。”用这些药物进行常规治疗会迅速削弱心肌的力量。“我们的研究结果现在表明,不是抑制PDE3,相反,选择性激活PDE3A可能是预防和治疗高血压引起的心脏损伤,如肥厚性心肌病和心脏衰竭Klußmann说。
但他说,在这发生之前,还需要对这种突变的保护作用有更多的了解。“我们已经观察到PDE3A不仅变得更活跃,而且它的浓度在心肌细胞他补充说,前者可能可以用寡聚化来解释,寡聚化是一种至少涉及两个酶分子共同作用的机制。“在这种情况下,”Klußmann说,“我们可能会开发出一些策略,人为地启动局部寡聚——从而模仿对心脏的保护作用。”
进一步探索