高体温改变autoinflammatory障碍的关键蛋白

从Garvan医学研究所的一项新的研究表明,核心体温的上升可能会导致炎症耀斑在患有ob欧宝直播nba一种罕见的基因疾病autoinflammatory。
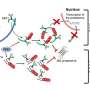
隐性障碍,称为甲羟戊酸激酶缺乏症(MKD),是由基因突变引起的甲羟戊酸激酶,必不可少酶存在于所有细胞在体内。缺乏这种酶会导致异常蛋白质的积聚,导致细胞免疫系统的故障,引发炎症。
这种情况通常出现在儿童早期,和病人的经验定期发作高发热和皮疹,溃疡,淋巴结肿大和腹痛。非常严重的疾病也会引起神经发育问题,可以是致命的。
“我们的研究提供了令人兴奋的新见解的潜在生理MKD可能引发炎症耀斑,开放潜在治疗这种毁灭性疾病的新方法,”Mike Rogers教授说,来自骨治疗实验室的主管。
这项新的研究发表在临床研究杂志》上。
”[有很少的研究进展,特别是MKD患者的疾病病因的耀斑。缺乏知识的一个主要原因是缺乏适当的动物模型来研究疾病的机制,“嘉芬的玛西娅穆尼奥斯博士说,该研究的第一作者。
团队使用基因编辑方法开发新的小鼠模型模拟代谢突变出现在原本的病人。“增加核心体温举例来说,这可能与压力或轻微感染发生,恶化突变酶的影响,导致戏剧性的异常蛋白质的积聚。这是一个可能导致患者炎症的耀斑,“穆尼奥斯博士说。
为什么原本有一个广泛的疾病严重程度知之甚少。“疾病是由突变基因的两个副本,有超过250种已知的突变,所以很难预测MKD的组合会导致轻微或严重版本,”罗杰斯教授说。
研究人员开发了不同的突变组合模型的疾病酶活性在10%或20%正常的水平。
“我们发现有一个阈值的酶活性。在20%左右活动,没有疾病。疾病开始出现如果酶活性低于这个阈值,当对蛋白质的影响,”罗杰斯教授说。
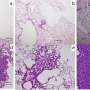
老鼠有20%的酶活性有非常轻微的疾病,而动物10%活动有明确的疾病和更高水平的异常蛋白质的迹象。
重要的是,提高体温降低酶活性几乎检测不到的水平,从而导致很高的异常蛋白质。
“我们可以开始使用这些信息预测;例如,通过测量的异常蛋白质水平的血液样品我们可以预见到症状的严重性”罗杰斯教授说。“临床医生可以用这些知识来帮助诊断和管理疾病。”
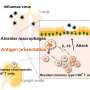
重要的是,研究人员还发现,蛋白质叫NLRP3 MKD的炎症过程中扮演了重要的角色。由于其参与多种炎症性疾病,目前主要的兴趣发展NLRP3阻滞剂在诊所使用。这一发现表明,针对NLRP3可能是[治疗的新方法。
娜塔莉台球的欢迎新发现,父母的一个13岁的女孩生活在一种罕见的autoinflammatory疾病被诊断为婴儿。“五十年前我女儿的病被称为“不兼容的生活。我们已经走过了漫长的道路由于人们喜欢罗杰斯教授和研究他的团队正在做的事情。这是生活给我们的孩子一个机会,”她说。