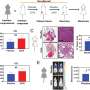
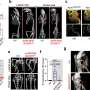
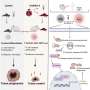
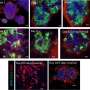
TP53/ rb1缺陷mCRPC中Enz耐药需要JAK-STAT信号。一个根据GSEA分析,热图表示LNCaP/AR细胞系经注释shRNAs转导后信号通路的显著变化。提出了三个比较。读取从n=每组3个独立处理的细胞培养物用于分析。信号通路同时改变TP53/RB1损失和SOX2上调用红色括号标示。b在由Cas9和注释引导rna转导的LNCaP/AR细胞中,JAK-STAT信号通路中激活的典型基因的相对基因表达;n= 3个独立处理的细胞培养物。P数值计算采用双向方差分析和Bonferroni多重比较检验。c,用Cas9和注释的CRISPR引导rna转导的LNCaP/AR细胞的相对细胞数。用10µM Enz处理细胞8 d,用CellTiter-Glo法测定细胞数量(活力),所有数值归一化为sgTP53/RB1组;n= 3个独立处理的细胞培养物。P计算值采用单因素方差分析(one-way ANOVA), Bonferroni多重比较检验;RLU,相对光单位。d,用Cas9和注释的CRISPR引导rna转导的LNCaP/AR细胞的相对细胞数。用10µM Enz处理细胞8 d,用CellTiter-Glo法测定细胞数量(活力),所有数值归一化为sgTP53/RB1组;n= 3个独立处理的细胞培养物。P计算值采用单因素方差分析(one-way ANOVA), Bonferroni多重比较检验;NS,不重要。eCas9和注解导向rna转导的LNCaP/AR细胞在去势小鼠体内的肿瘤生长曲线。Cas表示移植前2周阉割。Enz表示Enz处理为10 mg kg1从嫁接的第一天起;n=每组独立的异种移植瘤数量(每只小鼠2个肿瘤);sgNT,n= 8肿瘤;sgTP53 / RB1,n= 12肿瘤;sgTP53 / RB1 / JAK1,n= 8肿瘤;sgTP53 / RB1 / STAT1,n= 12肿瘤。P数值计算采用双向方差分析和Bonferroni多重比较检验。f注释的异种移植瘤载片上的JAK-STAT蛋白的免疫组化染色显示典型的肿瘤图像n= 2个独立肿瘤。信贷:自然癌症(2022)。DOI: 10.1038 / s43018 - 022 - 00431 - 9
TP53/ rb1缺陷mCRPC中Enz耐药需要JAK-STAT信号。一个根据GSEA分析,热图表示LNCaP/AR细胞系经注释shRNAs转导后信号通路的显著变化。提出了三个比较。读取从n=每组3个独立处理的细胞培养物用于分析。信号通路同时改变TP53/RB1损失和SOX2上调用红色括号标示。b在由Cas9和注释引导rna转导的LNCaP/AR细胞中,JAK-STAT信号通路中激活的典型基因的相对基因表达;n= 3个独立处理的细胞培养物。P数值计算采用双向方差分析和Bonferroni多重比较检验。c,用Cas9和注释的CRISPR引导rna转导的LNCaP/AR细胞的相对细胞数。用10µM Enz处理细胞8 d,用CellTiter-Glo法测定细胞数量(活力),所有数值归一化为sgTP53/RB1组;n= 3个独立处理的细胞培养物。P计算值采用单因素方差分析(one-way ANOVA), Bonferroni多重比较检验;RLU,相对光单位。d,用Cas9和注释的CRISPR引导rna转导的LNCaP/AR细胞的相对细胞数。用10µM Enz处理细胞8 d,用CellTiter-Glo法测定细胞数量(活力),所有数值归一化为sgTP53/RB1组;n= 3个独立处理的细胞培养物。P计算值采用单因素方差分析(one-way ANOVA), Bonferroni多重比较检验;NS,不重要。eCas9和注解导向rna转导的LNCaP/AR细胞在去势小鼠体内的肿瘤生长曲线。Cas表示移植前2周阉割。Enz表示Enz处理为10 mg kg1从嫁接的第一天起;n=每组独立的异种移植瘤数量(每只小鼠2个肿瘤);sgNT,n= 8肿瘤;sgTP53 / RB1,n= 12肿瘤;sgTP53 / RB1 / JAK1,n= 8肿瘤;sgTP53 / RB1 / STAT1,n= 12肿瘤。P数值计算采用双向方差分析和Bonferroni多重比较检验。f注释的异种移植瘤载片上的JAK-STAT蛋白的免疫组化染色显示典型的肿瘤图像n= 2个独立肿瘤。信贷:自然癌症(2022)。DOI: 10.1038 / s43018 - 022 - 00431 - 9
德克萨斯大学西南分校的科学家们领导的一项研究表明,阻止前列腺癌细胞转变为其他类型的细胞可以克服它们对广泛处方疗法产生的耐药性。研究结果发表在自然的癌症,这种致命疾病是美国男性中第二大常见癌症,每年导致近3.5万人死亡
“我们认为这种新颖的联合疗法可以显著改善前列腺癌患者的临床结果,并有望挽救许多生命,”研究负责人、分子生物学助理教授、哈罗德c西蒙斯综合癌症中心成员穆平博士说。
针对雄性激素受体(AR)是一种前列腺发育和维持的关键蛋白质,近几十年来,它已经彻底改变了前列腺癌的治疗,延长了数十万患者的生命。然而,穆医生解释说,随着时间的推移,这些疗法会失败,因为前列腺肿瘤会对它们产生耐药性。
在过去的五年里,穆博士和其他癌症研究人员发现,这些肿瘤产生耐药性的一个原因是通过一种称为谱系可塑性的现象,即恶性前列腺细胞恢复到发育的早期阶段,并具有新的特性,成为不再依赖于AR的不同细胞类型。尽管谱系可塑性已在其他癌症类型中被发现,包括肺癌、乳腺癌和黑色素瘤,它背后的分子机制在很大程度上仍然未知,阻碍了开发防止耐药性形成的疗法的努力。
为了更好地理解是什么推动了谱系的可塑性和耐药性,穆博士和他的同事们使用多个实验室模型对对ar靶向药物具有耐药性和敏感性的细胞进行了比较:在培养皿中生长的人类前列腺癌细胞系,模仿自然前列腺癌结构的人和小鼠前列腺癌细胞组成的三维“类器官”,以及前列腺癌的小鼠模型。研究人员使用不同的分析方法,包括单细胞RNA测序,寻找将耐药细胞从敏感细胞中分离出来的关键分子途径。
他们的研究揭示了一个被称为Janus激酶信号转换器和转录激活器(JAK-STAT)的特殊信号通路,似乎驱动着谱系的可塑性和抗性。当研究人员使用一种基因技术分别敲除构成这一通路的11个主要基因时,他们发现JAK1和STAT1基因在这些现象中起着关键作用。消除这些基因会使已经转变为新细胞类型的前列腺癌细胞恢复到原来的状态,并对当前的治疗再次敏感。
穆博士解释说,用抑制这些基因的药物治疗癌细胞也有类似的效果,不仅结束了它们的谱系可塑性,还使它们对ar靶向疗法重新敏感。当耐前列腺癌细胞如果同时使用JAK1和STAT1抑制剂和ar靶向药物,这些癌细胞就会失去分裂和生存的能力。
穆博士说,使用类似的策略可以提供一种克服人类前列腺癌患者耐药性的新方法,他和同事们计划最终在临床试验中测试这种方法。
更多信息:Su Deng等人,异位JAK-STAT激活使其过渡到茎状和多谱系状态,从而产生ar靶向治疗耐药性,
自然癌症(2022)。
DOI: 10.1038 / s43018 - 022 - 00431 - 9
引用:预防前列腺癌细胞中的“身份盗窃”使其对治疗重新敏感(2022年,10月18日),从//www.puressens.com/news/2022-10-identity-theft-prostate-cancer-cells.html获得2022年10月20日
本文件受版权保护。除用于个人学习或研究的公平交易外,未经书面许可,不得转载任何部分。内容仅供参考之用。