流感病毒及其对血液干细胞和凝血功能的影响
病毒引起的呼吸道感染可能危及生命。保罗-埃利希研究所(paul - ehrlich - institute)的一个研究小组与海德堡的研究人员一起发现,仅限于肺部的流感病毒感染也会导致血液干细胞的激活和血小板形成的增加。血小板可导致血栓形成,正如COVID-19的严重病例所显示的那样。信使物质白细胞介素-1和白细胞介素-6参与了激活。细胞的报道从2022年10月4日开始在其在线版本中记录结果。
每年冬季都会爆发不同强度的流感。它们是由流感病毒引起的。严重的流感感染病例与免疫系统脱轨有关细胞因子风暴伴随信使物质(细胞因子)的过度释放,而引起损伤肺细胞.感染可导致血管渗漏并引起血栓。这些反应类似于由SARS-CoV-2冠状病毒引起的COVID-19严重病例。严重病例是什么时候发展起来的?发生这种情况时会发生什么过程?许多细节都是未知的。
严重流感病例的并发症包括流感病毒的数量减少和增加血小板在血液中,这可能与增加的机会有关血栓形成.由paul - ehrlich - institute“干细胞基因修饰”研究小组负责人Ute Modlich教授领导的研究人员与德国癌症研究中心(DKFZ)海德堡和海德堡大学的科学家们在一个研究网络中进行了合作,研究癌症与干细胞之间的关系流感病毒感染(H1N1)和血液或血小板的形成。H1N1流感病毒是德国每年传播的流感病毒之一。
流感病毒感染肺部及其对血液形成的影响
所有的血细胞,因此所有的血小板都是由可以发展成血细胞(造血干细胞,HSCs)的干细胞更新的。这些细胞以静息状态存在于骨髓中。造血干细胞的命运在休止、自我更新和分化之间受到严格调控,以确保终身造血。
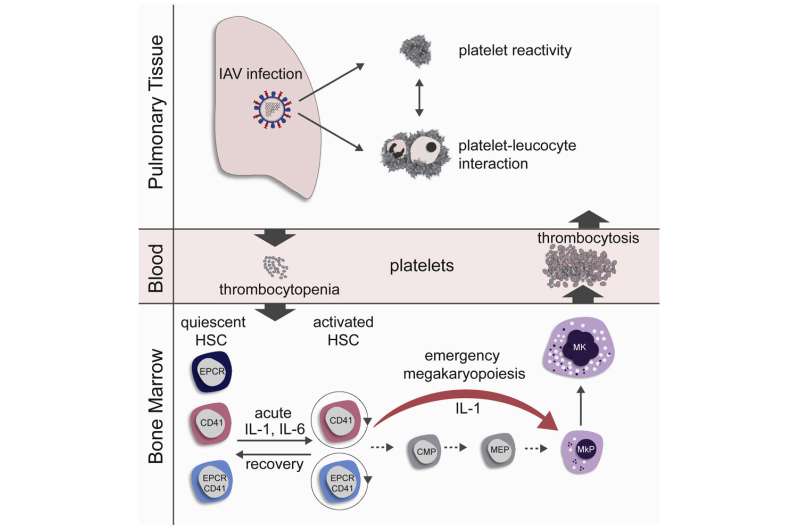
为了研究流感病毒感染对血液形成的影响,我们在小鼠鼻内感染流感病毒,然后研究它们的血液干细胞的分化和细胞周期激活。在急性流感感染的头三天,血小板最初减少(血小板减少),但随后在血液中迅速上升到高于生理水平(血小板增多)。这些快速产生的血小板具有不成熟的外观(表型)和更快速的激活(超反应)。
在感染后2天的成熟过程中(G1和S/G2/M细胞周期阶段)发现血干细胞数量增加。血干细胞的激活与病毒肺滴度呈正相关,即攻击肺部的病毒越多,血干细胞被激活的越多。减少流感剂量的感染延迟了干细胞的激活,但不能预防。在再生期,血液干细胞恢复到静止期。这在接种疫苗的小鼠中比其他组发生得更快。
具有典型血小板前体标记的血液干细胞
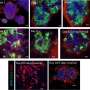
为了弄清血小板是如何如此迅速地产生的这个问题,研究小组仔细观察了激活的血液干细胞的表型,发现一部分血液干细胞已经携带了血小板前体细胞的典型标记(巨核细胞).具有这种表面表型的血液干细胞直接分化为巨核细胞并产生血小板。他们跳过了前面的几个阶段。研究小组通过体外血统追踪和骨髓移植证实,流感感染后,这组血干细胞在骨髓中迅速繁殖。这些新产生的血小板比普通血小板更大,外观更不成熟,而且往往更容易激活,这可能导致肺部血栓的风险更高。
巨核细胞的快速分化过程确实已经被描述为紧急巨核生成,它发生在对全身炎症或感染的反应中。然而,到目前为止,没有怀疑与当地病毒性呼吸道疾病有关。尽管流感病毒在小鼠中的感染仅限于呼吸道,但在感染小鼠的骨髓中发现了白细胞介素-1 (IL-1)和白细胞介素-6 (IL-6)细胞因子水平的升高。使用两组敲除小鼠,一组关闭IL-1受体,一组关闭IL-6受体,研究小组证明,这些细胞因子对激活造血干细胞紧急巨核生物流感感染。
目前的数据显示,即使是局部(非全身性)病毒感染也会导致骨髓中血液形成的改变。在这一过程中形成的血小板会导致更高的血栓风险,尤其是在反应过度状态下的肺部。这可能会对真实的流感病例产生重大影响。
进一步探索