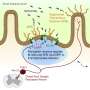
模型演示了RNA剪接缺陷如何导致阿尔茨海默病
研究人员使用他们的新模型来发现RNA剪接缺陷是如何导致阿尔茨海默病的神经退行性变的。RNA剪接是一种去除非编码基因序列并将蛋白质编码序列连接在一起的过程。
“RNA剪接是转录和翻译中必不可少的一步,”通讯作者彭俊敏博士说,他是圣犹大大学结构生物学和发育神经生物学系、蛋白质组学和代谢组学中心的博士,领导了这项研究。“这在大脑中尤为重要,因为我们知道大脑的细胞多样性比身体其他任何器官都要多,而剪接被认为是产生蛋白质多样性的重要过程。”
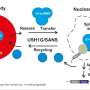
彭之前的工作揭示了RNA剪接机制的一个特殊成分,称为U1小核核糖核蛋白(snRNP),在阿尔茨海默症患者的大脑中产生聚集物。U1 snRNP复合体在RNA剪接中是必不可少的。
现在,彭和他的团队已经证明了U1 snRNP的功能障碍有助于神经退行性变,为阿尔茨海默症的治疗开辟了新的研究途径。研究发现,由于U1 snRNP病理导致的RNA剪接功能障碍有助于导致神经退行性变。
彭说:“我们之前的工作表明,U1 snRNP是大脑中形成缠结状结构的一种聚集体,但这只是描述性的,直到现在我们还不了解这种病理与疾病表型之间的联系机制。”
独特的模型将RNA剪接缺陷与神经元超兴奋性联系起来
研究人员创建了一种名为N40K-Tg的RNA拼接缺陷小鼠模型。当科学家们解除对剪接机制的控制时,他们观察到了基本的神经退行性变,但他们想了解为什么会这样。
彭说:“拼接机械是如此重要,在实验室中创建一个模型来研究它是一个真正的挑战。”“我们能够创建一个只发生在神经元中的拼接功能障碍模型。这个模型证明了剪接功能障碍会导致神经元毒性和认知障碍。”
抑制神经元活动可以防止大脑过度兴奋。如果科学家抑制抑制神经元的活动,神经元会变得更活跃,但它会导致毒性。研究人员发现了对突触蛋白的显著影响,特别是与抑制神经元活动有关的蛋白质。
“兴奋性毒性非常重要,因为在阿尔茨海默病领域已经知道了,”彭说。“甚至在20-30年前,人们就认识到神经元变得超级兴奋,现在我们发现,剪接机制可能是导致阿尔茨海默症患者兴奋性毒性的原因。”
RNA剪接缺陷和β-淀粉样蛋白聚集结合
阿尔茨海默病的一个标志是大脑中β-淀粉样蛋白和tau蛋白的聚集。Peng之前的工作揭示了U1 snRNP在大脑中也会形成聚集物,但科学家们无法研究U1 snRNP功能在疾病中的作用,直到他们开发了一个扰动U1 snRNP功能导致RNA拼接缺陷的模型。
为了了解RNA剪接缺陷在β-淀粉样蛋白聚集情况下的行为,研究人员将他们的小鼠模型与β-淀粉样蛋白模型交叉。这两种类型的毒性攻击一起重塑了大脑的转录组和蛋白质组,解除了对突触蛋白质的调控,加速了认知能力的下降。
从最初的行为到细胞生物学现在来看看分子机制,我们已经描述了RNA的潜在贡献拼接机械对阿尔茨海默病神经元兴奋性毒性的影响,”彭说。
这种交叉小鼠模型与早期的模型相比,更接近于人类的阿尔茨海默症,这可能有助于未来对该疾病的研究。