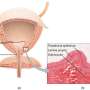
毒性数据显示S/N1806膀胱癌试验没有安全性问题
正在进行的SWOG/NRG 1806临床试验更新了毒性数据,该试验测试了在局限性肌肉浸润性膀胱癌患者中联合放化疗和免疫治疗,结果显示该联合疗法没有显著的安全性问题。
S/N1806研究小组成员、德克萨斯州坦普市贝勒斯科特和怀特健康公司的医学博士Sameer G. Jhavar将于10月25日在圣安东尼奥举行的2022年美国放射肿瘤学会(ASTRO)年会上口头报告213例患者的安全性报告。
参加S/N1806期临床试验的患者均为非转移性肌肉侵袭性膀胱癌。所有参与试验的患者被随机分为两个治疗组,比例为1:1。两臂患者均采用标准的三联疗法,即结合内镜手术最大限度地切除膀胱肿瘤和放化疗。研究组的一半患者还接受免疫治疗药物atezolizumab与放化疗结合,每三周一次,持续六个月。
该报告的主要作者是帕明德·辛格,医学博士,亚利桑那州凤凰城梅奥诊所的SWOG研究员。
辛格说:“这是一项随机的三期临床试验,研究在保留膀胱的三模态放化疗中加入免疫疗法。”“在研究组中没有明显的毒性问题,这表明该方案是安全的,试验继续积累得非常好。如果结果为阳性,该试验可能会改善患有糖尿病的患者的治疗方案膀胱癌这样他们就能保护自己的膀胱。”
在接受评估的213例患者中,113例接受了三模态治疗+ atezolizumab联合治疗。剩下的100名患者被随机分配到三模态治疗的控制组。
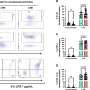
总体而言,atezolizumab组113例患者中有65例(58%)报告了3级或更高级别的毒性,而对照组100例患者中有44例(44%)报告了3级或更高级别的毒性。大多数毒性是血液学的,治疗医师认为与免疫无关。然而,已知一些与免疫相关的不良事件atezolizumab被报告为3级或更高的研究组。
早期对前80名纳入试验的患者的预先指定的安全性分析也显示无显著增加毒性在研究组和控制组进行比较。S/N1806试验持续积累良好,预计在未来两年内达到475例患者的入组目标。这是北美最大的膀胱保留疗法研究。