切换轨迹:改变肝脏中胰高血糖素受体的运输可以调节其代谢信号
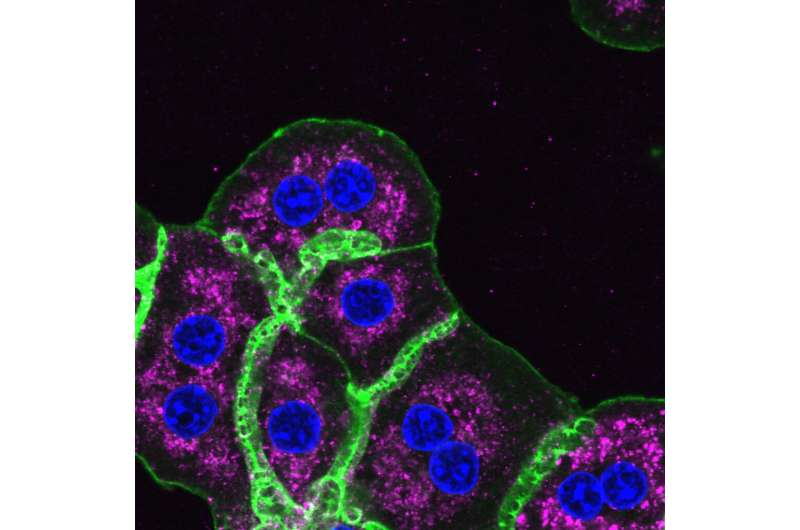
来自赫姆霍尔兹慕尼黑糖尿病和癌症研究所(IDC)的一组研究人员揭示了一种通过改变细胞内运输来改变肝脏中胰高血糖素受体信号的新策略。胰高血糖素是一种肽激素,负责血糖平衡,从而调节血糖水平。这种新方法通过解耦胰高血糖素的葡萄糖和脂质代谢相关效应,为2型糖尿病的治疗提供了治疗潜力。
在禁食期间,荷尔蒙胰高血糖素在体内循环,开始释放和分解储存的物质葡萄糖还有肝脏的脂质来提供能量。两者是否和如何使用能源(葡萄糖和脂类)是否能独立被激活,目前尚不清楚。Revathi Sekar, Karsten Motzler及其同事发表在细胞代谢现在发现,从肝脏中消耗蛋白质Vps37a会改变细胞内胰高血糖素受体的定位,从而在不影响脂质的情况下激活细胞内膜上的葡萄糖代谢。
Vps37a控制胰高血糖素受体在细胞中的运输
肝脏是维持空腹血糖水平平衡的主要器官,它通过外界信号(如胰高血糖素)释放储存的葡萄糖。然而,在2型糖尿病中,这一途径过度激活,导致肝脏产生葡萄糖,尽管已经很高血糖水平.这种血液中葡萄糖水平过高的情况被称为高血糖症。对胰高血糖素在肝脏中的作用进行药理抑制已被证明是具有挑战性的,因为胰高血糖素不仅调节葡萄糖的产生,而且还介导肝脏脂质分解。
因此,阻断胰高血糖素的作用承载着脂质的积聚肝作为负面副作用。由国际数据中心的组长Anja Zeigerer博士领导的研究团队,现在已经找到了一种可能的方法,通过干扰胰高血糖素受体的细胞内定位和信号通路,断开这两种途径,从而恢复胰高血糖素拮抗剂作为2型糖尿病的潜在治疗方法。
需要新的治疗方案
肥胖和相关的2型糖尿病患病率正在显著增加。然而,由于不是每个患者对现有疗法的反应都一样好,更多治疗方案是必需的。
第一作者Revathi Sekar和Karsten Motzler及其同事的研究提供了一种优雅的方法,通过抑制胰高血糖素有效降低血糖,而不需要脂质有关的副作用。