研究表明,肠道中的耐抗生素微生物使艰难梭菌更具传染性
艰难梭状芽胞杆菌(Clostridioides difficile),通常被称为艰难梭菌或C. diff,是一种会导致严重肠道疾病的细菌,顾名思义,很难研究和治疗。大约六分之一感染艰难梭菌的患者会在两个月内再次感染。然而,科学家们还没有弄清楚为什么艰难梭菌感染在某些患者身上比其他患者更难治疗。
人体肠道充满了数万亿微生物,这些微生物会影响各种病原体的毒力,但直到现在,科学家们对艰难梭菌如何与胃肠道中丰富的微生物群合作还知之甚少。
在一项新的研究中自然费城儿童医院(CHOP)的研究人员发现,肠球菌(一种耐抗生素的机会性病原体)与艰难梭菌共同作用,重塑和增强肠道的代谢环境,以便艰难梭菌能够茁壮成长。
“当我们谈论细菌感染时,我们通常只想到病原体本身,但肠道中的‘旁观者’可能对感染过程产生巨大影响,”费城儿童医院病理学和实验室医学研究员兼助理教授、资深作者Joseph P. Zackular博士说。
“这项研究揭示了两种致病菌——肠球菌和艰难梭菌——的巧合不仅仅是巧合;他们真的是在利用对方。了解这种关系,以及影响艰难梭菌感染临床结果的其他因素,对于应对这一紧迫的公共卫生挑战至关重要。”
先前的研究表明,感染艰难梭菌的成年人肠道中也有高水平的肠球菌,而万古霉素耐药肠球菌(VRE)经常同时感染艰难梭菌患者。然而,肠球菌对艰难梭菌感染易感性和临床结果的影响尚未确定。
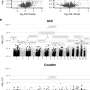
为了进一步确定肠球菌和艰难梭菌感染之间的关系,研究人员分析了54名感染艰难梭菌的儿童患者的粪便样本。与成年人的研究一致,研究人员发现这些患者的粪便中肠球菌含量高,肠球菌和艰难梭菌负担呈正相关。
在确认肠球菌在艰难梭菌感染儿童的肠道中高度丰富,并且这与艰难梭菌负担呈正相关后,研究人员随后验证了这两种病原体如何共同作用的机制。通过体外和体内实验模型,他们发现肠球菌通过增加毒素的产生来增加艰难梭菌的毒性。
然后,利用从转录组学到代谢组学的数据,即对与这些病原体相关的RNA转录物和代谢物的研究,研究人员发现肠球菌重塑了肠道环境,有效地重塑了艰难梭菌病原体进入的房子,使其更有利于病原体的生长。
他们发现肠球菌使用精氨酸(一种氨基酸)作为能量,在此过程中,病原体输出另一种氨基酸鸟氨酸。进一步的分析表明,肠球菌在艰难梭菌感染期间调节肠道中精氨酸和鸟氨酸的水平,精氨酸的消耗在艰难梭菌的毒性中起着核心作用。
最后,研究人员探讨了他们在实验室中的发现是否与人类患者的发现相关。通过分析艰难梭菌感染和炎症性肠病(IBD)儿童的微生物群,他们发现这些儿童具有高水平的可发酵氨基酸,包括鸟氨酸。他们还观察到艰难梭菌负担和鸟氨酸之间的正相关,支持这种氨基酸在艰难梭菌感染中的关键作用。
“总的来说,这些数据表明,肠球菌和艰难梭菌在艰难梭菌感染期间通过代谢交叉作用相互作用,以支持增加定植、发病机制和在肠道中的持久性,”扎克勒博士说。“未来的研究应该探索以肠球菌代谢为目标——以及由此产生的肠道氨基酸格局——作为改变艰难梭菌发病机制的一种方式。”