生物化学家和癌症生物学家发现了罕见脑瘤的关键弱点
自从她的职业生涯开始以来,Jennifer DeLuca一直着迷于有丝分裂,细胞分裂的日常生物过程:它是如何工作的,哪些蛋白质和细胞机制参与其中,以及为什么它有时会出错并导致疾病。
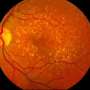
大约十年前,科罗拉多州立大学生物化学和分子生物学系的教授与癌症研究人员建立了合作关系,这些研究人员试图了解胶质母细胞瘤等癌症的生物学机制,胶质母细胞瘤是一种罕见的脑肿瘤。事实证明,调节有丝分裂的蛋白质,被称为着丝粒激酶(deluca的最爱),可以在决定是否有丝分裂中发挥重要作用癌症细胞要么增殖,要么死亡。这一发现使得DeLuca以有丝分裂为中心的基础研究成为癌症生物学家应用工作的完美补充。
DeLuca和她现在长期的癌症研究合作者,Fred Hutchinson癌症研究中心的Patrick Paddison一起,开始研究胶质母细胞瘤肿瘤病理学中与有丝分裂相关的蛋白质BubR1。他们观察到,当这种蛋白质从实验室培养的患者肿瘤细胞中消耗殆尽时,癌细胞就无法存活。他们想知道原因。
现在,他们发表在美国国家科学院院刊详细了解为什么某些癌症,包括与胶质母细胞瘤相关的癌症,对BubR1蛋白的缺失敏感。他们的工作使人们关注到这种或其他相关蛋白质被改造成靶向癌细胞但对癌细胞无害的生物药物的潜力正常细胞.
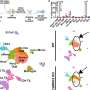
MAP激酶通路过度活跃
包括胶质母细胞瘤在内的许多癌症的发生,都是因为一种被称为丝裂原活化蛋白激酶通路的细胞信号传导过程变得过度活跃。这导致着丝粒激酶蛋白的过度活性,从而削弱了允许有丝分裂发生的附着。这些减弱的附着使癌细胞突然需要一种特殊的蛋白质——bubr1的帮助来继续分裂。健康的细胞没有这种脆弱性,使它们能够安全地忽略BubR1。
DeLuca的最新工作表明,消耗这种蛋白质或蛋白质生化途径上的任何参与者,对于任何与过度活跃的丝裂原激活蛋白激酶途径相关的癌症,包括胶质母细胞瘤,都是有希望的药物靶点。
DeLuca说:“这就是为什么将基础研究与癌症和转化研究结合起来是如此重要。”“如果你击中了一个蛋白质在美国,它可能无法作为一种治疗方法。但如果你知道整个通路的生物学原理,那么你就可以尝试击中很多不同的目标。”
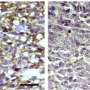
用病人肿瘤细胞,培养细胞做实验
前研究生雅各布·赫尔曼(Jacob Herman)进行了大部分实验,这些实验涉及细胞生物学技术,涉及患者肿瘤细胞、人类培养的细胞、实验室转化的细胞和小鼠培养的细胞。该团队还使用了CSU合作者和论文合著者Erin Nishimura实施的全基因组大数据技术,以帮助他们确定使癌细胞容易受到某些蛋白质抑制的微妙变化。
DeLuca说:“总的来说,这项工作扩展了我们对染色体分离和癌症生物学如何交叉的理解,并强调了探索不同细胞状态下有丝分裂过程的必要性。”