开发一种基于自然杀伤细胞的有前途的癌症新疗法
Keytruda和Opdivo等免疫检查点抑制剂通过释放免疫系统的T细胞来攻击肿瘤细胞。十年前,它们的引入标志着癌症治疗的重大进步,但只有10%到30%的接受治疗的患者经历了长期的改善。今天发表在临床研究杂志(江森自控),爱因斯坦医学院的科学家们描述了可能提高免疫检查点疗法有效性的发现。
爱因斯坦的研究小组并没有使用T细胞来对抗癌症,而是使用了不同的人免疫细胞被称为自然杀伤细胞(NK细胞)。
“我们相信,我们开发的新型免疫疗法有很大的潜力临床试验涉及各种类型的癌症,”研究负责人、医学博士邢星说。他是癌症研究的Louis Goldstein Swan Chair教授,也是爱因斯坦医学院微生物学与免疫学、肿瘤学、泌尿学和医学教授,也是蒙蒂菲奥里·爱因斯坦癌症中心癌症治疗学项目的成员。
分清朋友与敌人
免疫细胞的表面布满了被称为“检查点”蛋白质的受体,可以防止免疫细胞偏离它们通常的目标(病原体感染的细胞和免疫细胞)癌症细胞).当免疫细胞上的检查点受体与人体自身正常细胞表达的蛋白质结合时,这种相互作用就会阻止可能的免疫细胞攻击。可怕的是,大多数类型的癌细胞表达的蛋白质与检查点的蛋白质使免疫细胞停止攻击肿瘤。
免疫检查点抑制剂是一种单克隆抗体,通过阻断肿瘤蛋白或与肿瘤蛋白结合的免疫细胞受体来缩短免疫细胞/癌细胞的相互作用。在没有刹车的情况下,免疫细胞可以攻击并摧毁癌细胞。
对自然杀伤细胞的新关注
检查点抑制剂的有限效果促使臧博士和其他科学家研究涉及NK细胞的检查点通路,NK细胞和T细胞一样,在清除不需要的细胞方面发挥着重要作用。一种叫做PVR的癌细胞蛋白质很快引起了他们的注意。臧博士说:“我们意识到PVR可能是一种非常重要的蛋白质,人类癌症用它来阻碍免疫系统的攻击。”
PVR蛋白通常在正常组织中不存在或非常稀缺,但在许多类型的肿瘤中大量存在,包括结直肠癌、卵巢癌、肺癌、食道癌、头颈癌、胃癌、胰腺癌以及髓系白血病和黑色素瘤。
此外,PVR似乎通过与一种称为TIGIT的检查点蛋白结合来抑制T细胞和NK细胞的活性,从而通过使用TIGIT/PVR途径来中断TIGIT/PVR通路单克隆抗体对TIGIT。目前全球有100多项针对TIGIT的临床试验正在进行中。然而,一些临床研究包括两项大型三期临床试验,最近都未能改善癌症预后。
认识到新受体的作用
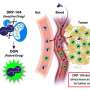
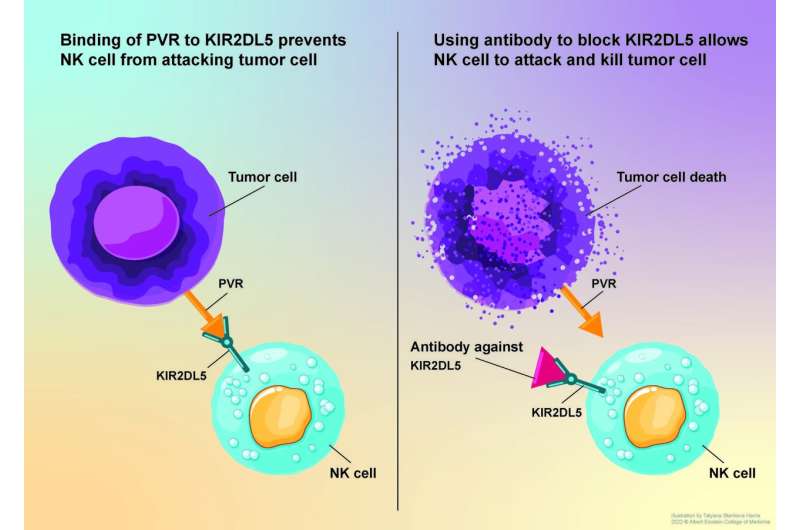
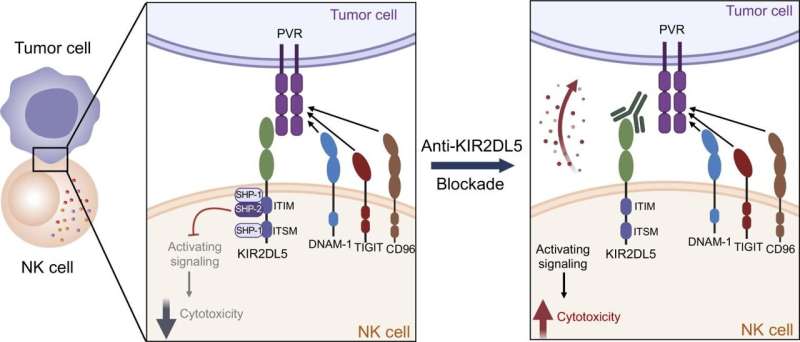
同时,癌细胞蛋白PVR被发现在NK细胞上有另一个“结合伙伴”:KIR2DL5。“我们假设PVR不是通过与TIGIT结合,而是通过与最近发现的KIR2DL5结合来抑制NK细胞的活性,”Zang博士说。为了找到答案,他和他的同事合成了一种针对KIR2DL5的单克隆抗体,并使用该抗体进行了体外和体内实验。
在他们的江森自控在论文中,臧博士和同事们证明了KIR2DL5是人类NK细胞表面常见的检查点受体,PVR癌症蛋白利用它来抑制免疫攻击。
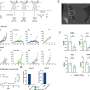
在涉及几种人类癌症的人源化动物模型的研究中,研究人员表明,他们针对KIR2DL5的单克隆抗体-通过阻断KIR2DL5/PVR通路-允许NK细胞大力攻击和缩小人类肿瘤并延长动物生存(见附图)。臧博士说:“这些临床前研究结果提高了我们的希望,即靶向KIR2DL5/PVR途径是一个好主意,我们开发的单克隆抗体可能是一种有效的免疫疗法。”
爱因斯坦提出了专利申请用于KIR2DL5/PVR免疫检查点,包括抗体药物,并有兴趣与合作伙伴进一步开发和商业化该技术。臧博士此前开发并申请了10多种免疫检查点抑制剂的专利。
其中一种抑制剂目前正在中国进行2期临床试验,涉及数百名晚期实体癌(非小细胞肺癌、小细胞肺癌、鼻咽癌、头颈癌、黑色素瘤、淋巴瘤)或复发/难治性血癌(急性髓系白血病、骨髓增生异常综合征)患者。又是张医生的免疫检查点抑制剂将于明年在美国的癌症临床试验中进行评估。