“CAR池”筛查可以识别最有效的癌症免疫治疗细胞
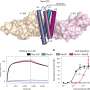
![Generation and screening of a pooled library of CARs with diverse signaling domains. (A) Our CARs combine an αCD19 ScFv (FMC63), a CD8 hinge and transmembrane domain (TMD), an intracellular signaling domain, and a CD3ζ domain (left). Forty domains from across the human proteome were codon-optimized, synthesized, pooled into a plasmid library, and packaged to generate lentivirus (right). These spanned protein families such as immunoglobulin superfamily (IgSF); T cell/transmembrane, immunoglobulin, and mucin (TIM); TNF receptor superfamily (TNFRSF); and triggering receptors expressed on myeloid cells (TREM). (B) Venn diagram showing natural expression of library members across immune cell types. Expression patterns are listed in table S1. NKT, natural killer T cell; DC, dendritic cell. (C) Primary human CD4 and CD8 T cells were separately isolated from PBMCs for two human donors and lentivirally transduced with the library. The cells were FACS-purified using T2A-GFP fluorescence within one log of mean expression to reduce variability. (D) The pooled library was repeatedly stimulated 1:1 with CD19<sup>+</sup> or CD19<sup>−</sup> irradiated K562 tumor cells to quantify antigen-specific activation (CD69), cytokine production (IFN-γ and IL-2), and proliferation [CellTrace Violet (CTV)]. The library was also sequenced at the specified time points to measure the relative expansion of individual constructs. (E) Percentage of CD8<sup>+</sup> T cells expressing different numbers of exhaustion markers (PD1, TIM3, LAG3, and CD39) after a repeat stimulation assay with CD19<sup>+</sup> irradiated K562 tumor cells. T cells expressing CD28, 4-1BB, or CD3ζ-only CARs are compared to untransduced (Untrans.) cells. Gray boxes correspond to time points in which no live cells remained. Significance was assessed in CD8 T cells for two donors using a repeated-measures ANOVA model. FDR-corrected *P = less than 0.05 and ***P = less than 0.001; ns, not significant. The second donor and data for CD4<sup>+ </sup> T cells are shown in fig. S1 (A and B). (F) We used FlowSeq, a FACS and next-generation sequencing-based pooled quantification workflow, to quantify enrichment by sorting the library into bins of fluorescent signal corresponding to a functional readout, as shown by the colored histograms. We then amplified the costimulatory domain by genomic DNA extraction and PCR and performed amplicon sequencing on each bin to estimate the phenotype for each library member. Credit: <i>Science Translational Medicine</i> (2022). DOI: 10.1126/scitranslmed.abm1463 “CAR池”筛查可以识别最有效的癌症免疫治疗细胞](https://scx1.b-cdn.net/csz/news/800a/2022/car-pooling-screens-id.jpg)
近年来,基因改造的免疫细胞——装备分子武器来识别和摧毁肿瘤细胞——已经改变了癌症治疗的前景。现在,加州大学旧金山分校的研究人员开发了一种新方法,可以比较大量的这些CAR-T细胞,每个细胞的分子特征略有不同,以确定哪种对癌症最有效、最持久。
他们在2022年11月9日发表的研究中科学转化医学在美国,该团队使用了一种被称为“CAR Pooling”的方法来研究40种不同的CAR- t细胞受体.在未来,这个屏幕可以扩展到测试数百或数千种受体组合,已经发现了新的和令人惊讶的受体,使这些治疗细胞更强大。
“CAR-T细胞对许多血癌患者来说绝对是革命性的,”资深作者、加州大学旧金山分校微生物学和免疫学副教授、格莱斯顿-加州大学旧金山分校基因组免疫学研究所成员Kole Roybal博士说。“这项工作是一个垫脚石,我们将以更聪明的方式设计这些细胞,让它们在更多类型的癌症中更好、更持久地工作。”
变革性治疗
T细胞是一种白细胞,在其表面表达受体,识别体内的外来物质。当一个匹配的分子或粒子适合T细胞受体时,细胞就会启动一个免疫反应为了抵御侵略者。这种反应不仅可以消灭病毒和细菌,而且还可以癌症细胞也
当癌症患者接受CAR-T细胞治疗时,临床医生从患者的血液或健康的供体中收集T细胞。然后,他们在实验室里改变这些细胞,加入DNA来诱导免疫细胞在其表面产生特殊的癌症识别嵌合抗原受体(CARs)。改造后的细胞被培养出来并注射回患者体内。新的car帮助T细胞特异性地攻击癌细胞。多种CAR-T细胞已被批准用于血癌,包括淋巴瘤、白血病和多发性骨髓瘤。
加州大学旧金山分校博士后学者、这项新研究的共同第一作者丹尼尔·古德曼博士说:“我们能够将T细胞从体内取出,向它们添加新的遗传程序,并将它们作为一种活的可编程疗法放回体内,这已经对血液癌症的治疗产生了巨大的影响。”“然而,如果我们更充分地了解如何操纵工程细胞的信号和功能特性,这只是工程细胞能力的开始。”
研究人员一直在努力让CAR-T细胞对抗实体肿瘤。即使对许多血癌患者来说,CAR-T细胞也只是暂时起作用,或者根本不起作用。
开发新的CAR-T细胞疗法的限制因素之一是修改和测试新受体所需的高通量技术;在整个免疫系统中,有数百个受体片段,它们可以像乐高积木一样组合成数千种可能的组合。
简化T细胞测试
Roybal、Goodman和共同第一作者camilia Azimi开发了CAR Pooling,以一次快速测试不同CAR的有效性。这种筛查的工作原理是生成一个包含许多免疫受体遗传密码的DNA库,同时将它们引入数百万个细胞,然后让这些细胞在试管中竞争它们在生存、生长、识别和摧毁癌症方面的技能。
“我们的方法使测试基于受体的新疗法的过程更快,”当时在加州大学旧金山分校读研究生的阿兹米说。“这不仅可以让研究人员节省时间,还可以探索他们无法单独测试的设计。”
例如,在这项新研究中测试的40种car中,不仅有经典的t细胞受体,还有从其他类型的相关免疫细胞借来的受体。例如,一种名为BAFF-R的b细胞受体是使T细胞特别有效地对抗癌症的主要竞争者。
Azimi说:“如果我们没有使用CAR Pooling,我们永远不会选择测试BAFF-R。
当含有BAFF-R的CAR-T细胞在患有多发性骨髓瘤的小鼠中进行测试时,与接受标准CAR-T细胞的小鼠相比,这些小鼠存活时间更长,患癌症的几率更低。
未来研究的平台
研究小组正计划扩大CAR - Pooling的应用,以测试再造T细胞中更多的受体。Roybal说,最终,这种方法可以用于开发针对不同类型癌症的不同种类的CAR-T细胞;当涉及到不同的癌症类型时,可能没有一个通用的答案。
他说:“我们当然可以使用CAR - Pooling来快速找到适合特定临床环境的最佳受体。”“一组受体可能对胶质母细胞瘤更有益,而另一组受体对骨髓瘤最有益。”
随着研究人员筛选越来越多的免疫受体,他们希望揭示受体如何支配免疫细胞活动的潜在模式。最终,这可能会导致更多的合成受体,可以接受不仅癌症,但其他疾病。
古德曼说:“我们希望了解如何组成这些信号域的基本部分,并建立下一代工程细胞疗法。”
该实验室还致力于了解和改进CAR-T细胞受体之外的其他方面,以提高治疗的有效性。
“有很多方法可以修改这些细胞,”Roybal说。“这只是拼图的一部分。”